
�������̼��ƺ�ϡ������ȡ������̼��ʵ�飬������ͼ��ʾ����������װ�ã��ش��й����⣺
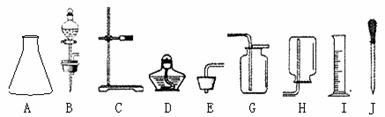
��1������Һ��������100g������������Ϊ10%��ϡ���ᣬ��Ҫ20%������ g����Ҫ����ˮ�����Ϊ ml����ѡ��____��ѡ�50ml����100ml������Ͳ��ȡˮ�IJ����У���ˮ��ӽ�����̶�ʱ��Ӧ���� �� ������ţ���ˮ������̶ȡ�
 ��2������ǩ�������ƺõ���Һװ���Լ�ƿ�У���������ͼ��ʾ�Ŀհױ�ǩ�������Լ�ƿ������ǩ�����ݡ�
��2������ǩ�������ƺõ���Һװ���Լ�ƿ�У���������ͼ��ʾ�Ŀհױ�ǩ�������Լ�ƿ������ǩ�����ݡ�
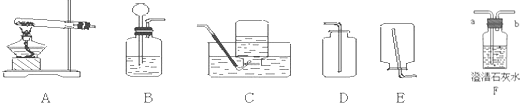
��3��ѡ��������̼��ƺ�ϡ������ȡ������̼���÷�Ӧ�Ļ�ѧ����ʽ�� ���䷢��װ�ú��ռ�װ�ÿ�ѡ����ͼ�е� ������ţ���ϣ�������ѡ��װ�������ѡ��һ������������������ ����Ҫ˵��������; ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ĩ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ������������ѧ���꼶���ϣ�������⻯ѧ�Ծ���12�·ݣ��������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com