
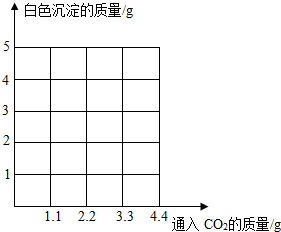
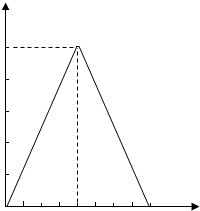
 小丰同学一次实验的意外发现:①向饱和澄清石灰水中逐渐通入C02,开始产生白色沉淀,并不断增多;②然后白色沉淀又不断减少,消失,溶液又变澄清.对此现象,小丰同学结合所学知识并查阅资料,找到了原因:现象①主要是因为随着C02的不断通入,与氢氧化钙反应生成了不溶于水的CaC03;现象②主要是因为CaC03+H20+C02═-=Ca(HC03)2,Ca(HC03)2易溶于水.以下是小丰同学的后续实验:
小丰同学一次实验的意外发现:①向饱和澄清石灰水中逐渐通入C02,开始产生白色沉淀,并不断增多;②然后白色沉淀又不断减少,消失,溶液又变澄清.对此现象,小丰同学结合所学知识并查阅资料,找到了原因:现象①主要是因为随着C02的不断通入,与氢氧化钙反应生成了不溶于水的CaC03;现象②主要是因为CaC03+H20+C02═-=Ca(HC03)2,Ca(HC03)2易溶于水.以下是小丰同学的后续实验:| 74 |
| 100 |
| 3.7 |
| X |
| 44 |
| 2.2 |
| 162 |
| m |
| 40 |
| 162 |
| 20 |
| 81 |
| 20 |
| 81 |


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:初中化学 来源: 题型:阅读理解

| ||
| 该同学的观点 | 请说出你的观点并阐述理由 |
| 该实验没有对氧气进行验证 | 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺. 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺. |
| “结论2”不正确 | 同意此观点.根据质量守恒定律,反应前后原子的种类和数目不变:反应前有氢原子,反应后又无氢气生成,所以应有水生成. 同意此观点.根据质量守恒定律,反应前后原子的种类和数目不变:反应前有氢原子,反应后又无氢气生成,所以应有水生成. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| 该同学的观点 | 请说出你的观点并阐述理由 |
该实验怎么没有对氧气进行验证 |
不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺. 不同意此观点.因为氧气具有助燃性,若有氧气产生,实验操作2中的木条燃烧的会更旺. |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年北京市房山区九年级第一学期终结性检测化学试卷 题型:探究题
在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中不断吹气,在吹气
的过程中发现石灰水先出现浑浊后又变澄清,他感到很意外。
小强又将纯净的CO2持续通入新制的澄清石灰水中,一段时间后,观察到的现象与上次相同。
(1)小强做第二次实验的目的是 。
(2)小强从老师那里得知:CO2能与CaCO3和H2O继续反应生成Ca(HCO3)2。由此小强推测出Ca(HCO3)2的一条物理性质是 。
(3)小强还想了解Ca(HCO3)2的化学性质。查阅资料后得知碳酸氢钙[Ca(HCO3)2]受热易分解,生成难溶性的化合物、气体等物质。他与同学们一起对碳酸氢钙受热分解后产物的成分进行了探究。
【提出猜想】
猜想1.生成的难溶性化合物可能是碳酸钙。经实验探究结论正确。
猜想2.放出的气体可能是O2、H2、CO、CO2 中的一种或几种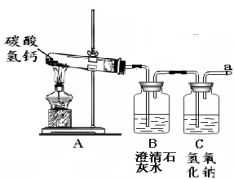

操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象。
【实验结论】
结论1.碳酸氢钙分解产生的气体一定有 。
结论2.碳酸氢钙受热分解的化学方程式为Ca(HCO3)2 CaCO3 ↓+ CO2↑
CaCO3 ↓+ CO2↑
【表达交流】
交流1.从安全的角度考虑,操作2实验中存在的不足是 。
交流2.小组内某同学对上述结论提出异议:
| 该同学的观点 | 请说出你的观点并阐述理由 |
| 该实验没有对氧气进行验证 | |
| “结论2”不正确 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
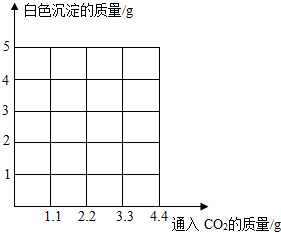 小丰同学一次实验的意外发现:①向饱和澄清石灰水中逐渐通入C02,开始产生白色沉淀,并不断增多;②然后白色沉淀又不断减少,消失,溶液又变澄清.对此现象,小丰同学结合所学知识并查阅资料,找到了原因:现象①主要是因为随着C02的不断通入,与氢氧化钙反应生成了不溶于水的CaC03;现象②主要是因为CaC03+H20+C02═-=Ca(HC03)2,Ca(HC03)2易溶于水.以下是小丰同学的后续实验:
小丰同学一次实验的意外发现:①向饱和澄清石灰水中逐渐通入C02,开始产生白色沉淀,并不断增多;②然后白色沉淀又不断减少,消失,溶液又变澄清.对此现象,小丰同学结合所学知识并查阅资料,找到了原因:现象①主要是因为随着C02的不断通入,与氢氧化钙反应生成了不溶于水的CaC03;现象②主要是因为CaC03+H20+C02═-=Ca(HC03)2,Ca(HC03)2易溶于水.以下是小丰同学的后续实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com