
| 编号 | 实验一 | 实验二 | 实验三 |
| 反应前 | 4.8g | 112.6g | 118.4g |
| 反应后 | 8.0g | 112.4g | 118.4g |
分析 质量守恒定律是指参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.要探究质量守恒定律,在比较反应前后的质量关系时,不可漏掉任何一种反应物或生成物.镁燃烧的实验中,参加反应的镁与氧气质量之和等于生成的氧化镁的质量,而实验一只称量了反应物镁的质量而没有称量参加反应的氧气的质量,从而导致实验数据增大.实验二中生成物有两种:氯化锌和氢气,参加反应的锌与盐酸质量之和等于生成的氯化锌和氢气的质量之和,而称量时漏掉了氢气的质量,导致数据减小.任何化学反应都应遵循质量守恒定律.为保证探究实验的成功,应在密闭容器中进行.
解答 解:(1)从表中可以看出,只有实验三反应前后数值相等;任何化学反应都遵循质量守恒定律,导致结果不守恒的原因是:实验一中漏掉了其中的反应物氧气,实验二中漏掉了生成物氢气,只比较了部分反应物或生成物的质量,所以从数值上得不出正确结论.
(2)实验三中无气体参加反应,也无气体生成,所以该实验能验证质量守恒定律;
(3)用实验研究化学反应前后反应物与生成物之间的质量关系时,要比较反应前后的“质量总和”,必须保证不能遗漏任何一种反应物与生成物,特别是有气体参与或生成的反应,故在密闭容器中实验是最可靠的.
故答案为:
(1)实验一反应前的质量总和还应包括参加反应的氧气的质量,实验二测定的生成物质量中少了另一种生成物氢气的质量;
(2)三;
(3)封闭.
点评 该题考查的是质量守恒定律的探究,实质是考查对质量守恒定律定义的理解,通常考查其中的“参加”、“质量总和”等,在作答时要找全反应物及生成物.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:初中化学 来源: 题型:选择题
| A. | 某固体中加入稀盐酸产生无色气体,证明该固体一定含有CO32- | |
| B. | 某溶液中增加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42- | |
| C. | 某无色溶液中滴加无色酚酞试液,溶液变成红色,该溶液不一定是碱 | |
| D. | 把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合金的熔点一般比组成它们的纯金属更高,抗腐蚀性能等也更好 | |
| B. | 铁锈是一种合金 | |
| C. | 合金中只含有金属元素 | |
| D. | 合金是一种混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子的质量很小 | B. | 不同分子性质不同 | ||
| C. | 分子不断运动 | D. | 分子间有间隔 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜和铁 | B. | 银和铁 | C. | 银和铜 | D. | 银 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
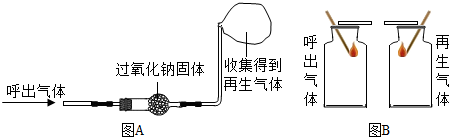

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com