
【题目】钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择低钠盐能实现减钠补钾。如图为某品牌低钠盐的标签。请你根据标签回答以下问题:

(1)氯化钾的相对分子质量为______;
(2)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克______?
(3)每500g该品牌的食盐中共含氯元素的质量是多少______?
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
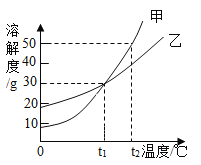
A. t1℃时,甲和乙的溶解度相等,都是30
B. t1℃时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等
C. 温度从t2℃降至t1℃时,甲和乙的饱和溶液中析出晶体的质量甲大于乙
D. t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于碳和碳的氧化物知识网络图(图中“→” 表示转化关系,“……”表示相互能反应)说法正确的是
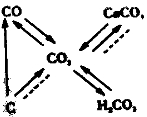
A.“C……CO2”的反应是放热反应
B.“CO→CO2”的反应类型为置换反应
C.“CO2→CaCO3”的反应可用于检验二氧化碳
D.“CO2![]() H2CO3”的反应可用酚酞试剂验证
H2CO3”的反应可用酚酞试剂验证
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.
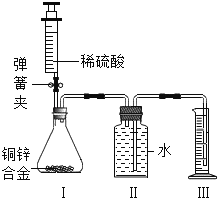
探究过程如下:
①连接实验装置并检查装置气密性.
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL.(注:样品中的杂质不参加反应)
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量1.4g.
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数.
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09g/L.
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为 ,实验过程中须加入稀硫酸至不再产生气体,目的是 .
(2)步骤③中称量剩余固体之前的正确操作是 、洗涤、干燥.
(3)根据实验测定的数据,上述三位同学中 (填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数.
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差.以下因素可能造成偏差的有 (填标号).
A.移出装置Ⅲ时,导管内留存了一部分水
B.实验测量前,没有排除装置Ⅰ中的空气
C.数据处理时,未排除加入稀硫酸所占的体积.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钠是人体必须的常量元素,其原子结构示意图和它在周期表中的相关信息如图所示。下列说法正确的是( )
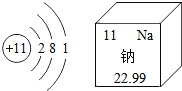
A.钠原子的相对原子质量为22.99gB.钠原子在化学反应中易失去电子
C.![]() 的核内质子数为10D.人体缺钠易导致骨质疏松
的核内质子数为10D.人体缺钠易导致骨质疏松
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生产和生活中有着广泛应用。
(1)下列金属制品在应用中,利用金属导热性的是_____
a.金属硬币 b.铜制火锅 c.铝制导线
(2)铝比铁活泼,但铝在空气中比铁稳定,其原因是_____
(3)工业上用盐酸除去钢板表面上的锈要严格控制盐酸的用量,用量过多会发生反应而损坏钢板,用化学方程式表示损坏钢板的反应_____
(4)高铁的迅速发展对钢轨的需求量越来越大,质量要求越来越高。工业上经常用“铝热反应”来焊接钢轨,其原理是:![]() ,该反应的基本类型是_____反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是_____kg
,该反应的基本类型是_____反应;若焊接钢轨需要50.4kg铁,理论上需要铝的质量是_____kg
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁合金是生产生活中使用最广泛的金属材料,但铁制品容易被腐蚀而在表面生成红褐色的铁锈。为探究铁制品锈蚀的条件,寻找防止铁制品锈蚀的方法,现进行如下实验:
步骤1:利用右图所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,将导管a、b处的止水夹k1、k2夹紧。
步骤2:一段时间后,观察U形管内三处铁丝表面的变化情况。
回答下列问题:
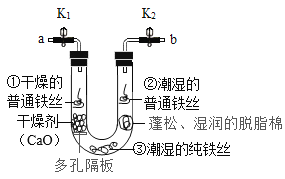
(1)步骤1中,检验U形管内已充满O2的方法是________。
(2)步骤2中,观察到①处没有明显变化,说明铁制品锈蚀的条件之一是需要有_______(填化学式),②处可能观察到的现象是_______,③处没有明显变化,说明纯铁的抗腐蚀能力较____(填“强”或“弱”)。
(3)待U形管内有明显现象后,将b导管插入水中,打开止水夹k2,观察到_____现象,说明该条件下铁制品锈蚀过程消耗了O2。
(4)通过上述实验现象,请你提出一种防止铁制品锈蚀的方法(不包括制造纯铁):__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学取10 g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7 g时,恰好完全反应,生成气体的质量与反应时间的关系如下图所示,试回答下列问题:
(1)完全反应后生成氢气的质量为 g。
(2)样品中锌的质量为多少克?
(3)反应后,所得溶液中硫酸锌的质量分数
为多少?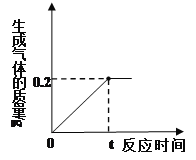
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com