
【题目】a、b、c 三种物质的溶解度曲线如下图所示。取等质量![]() ℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至
℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至![]() ℃。下列说法不正确的是
℃。下列说法不正确的是
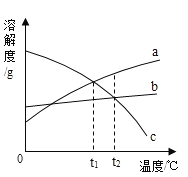
A. 原饱和溶液中,溶质的质量分数 a>b="c"
B. 恢复至 t2℃时,析出溶质的质量 a>b=c
C. 恢复至t2℃时,三种溶液一定都是饱和溶液
D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液
科目:初中化学 来源: 题型:
【题目】化学反应的实质是构成物质分子的原子重新进行组合,形成新分子的过程。如图是在密团容器中某化学反应过程的微观示意图。据图回答:
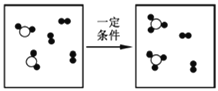
(1)参加反应的“![]() ”与“
”与“![]() ”的分子个数比为_________。
”的分子个数比为_________。
(2)该反应的基本反应类型是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中A~F是初中化学常见的物质,其中A和B都由两种相同的元素组成,C、D均为气体单质,气体C被誉为“二十一世纪最理想的能源”,单质E是目前世界年产量最高的一种金属,该金属在气体D中燃烧,火星四射,生成黑色固体F。
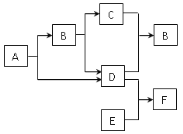
(1)写出下列物质的化学式:A______; C______;
(2)气体D在空气中的体积分数是_______%;
(3)写出金属E在气体D中燃烧的化学反应方程式___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
Ⅰ.(镍粉制备)
工业用电解镍新液(主要含NiSO4,NiCl2等)制备碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O],并利用其制备镍粉的流程如下:
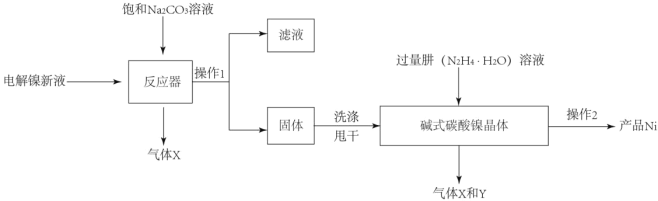
(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_____。
(2)物料在反应器中反应时需要控制反应条件。
分析下图,反应器中最适合的温度及pH分别为_____℃、_____。
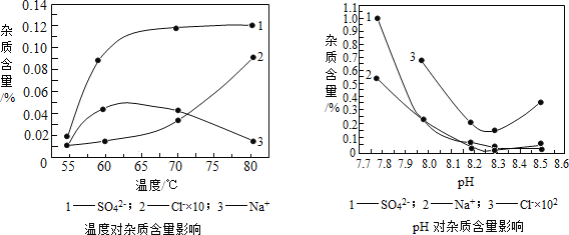
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将_____(填“升高”、“降低”或“不变”)。
(4)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是_____。
Ⅱ.(测定碱式碳酸镍晶体的组成)
为测定碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]组成,某小组设计了如下实验方案及装置:
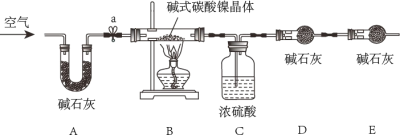
(资料卡片)
①碱式碳酸镍晶体受热会完全分解生成NiO、CO2和H2O
②碱石灰是NaOH和CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称量3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;
④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)
装置C/g | 装置D/g | 装置E/g | |
加热前 | 250.00 | 190.00 | 190.00 |
加热后 | 251.08 | 190.44 | 190.00 |
(实验分析及数据处理)
(1)实验过程中步骤⑤鼓入空气的目的是_____。
(2)计算3.77g碱式碳酸镍晶体[xNiCO3●yNi(OH)2●ZH2O]中镍元素的质量_____。最终通过计算得到了碱式碳酸镍晶体的组成。
(实验反思)
(3)另一小组同学加热时在酒精灯上加了铁丝网罩,实验结束后,称得装置B中残留固体质量明显增大。经查阅资料发现:在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3。该组同学称得残留的固体中镍元素的质量分数可能是_____。
A 70.1% B 75.9% C 78.7% D 79.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实验的基础上得出的。
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取干燥氢气的装置,正确的连接顺序为__(用接口处字母填写)。
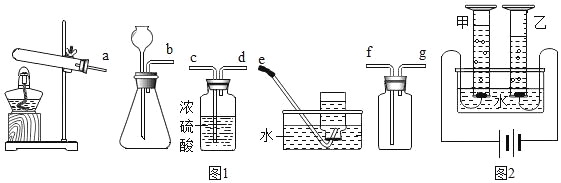
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要___;
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是___。
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。电解时,水中需加入少量的NaOH,其作用是__。通电一段时间后,发现甲、乙两量筒中收集的气体体积比略小于1:2,其原因可能是__(写出一条即可)。
(4)拉瓦锡还用另一实验证明了水的组成。他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】医院给病人输氧时用到类似如图所示的装置。关于该装置,下列说法不正确的是( )
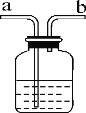
A. 输氧时,a导管连接供给氧气的钢瓶
B. 输氧时,该装置也能用来观测氧气输出的速率
C. 实验室中将该装置装满水收集氧气时,气体从a导管进入
D. 实验室中将该装置盛澄清石灰水时,气体从a导管进入可检验二氧化碳气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
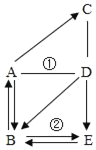
(1)物质C的化学式:_____;D→E反应的实质为_____。
(2)反应①的化学方程式:_____。
(3)反应②的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面材料,回答问题。
人类赖以生存的环境由自然环境和社会环境组成。自然环境由生物圈、岩石圈、大气圈、水圈组成(如图所示),四个圈层经过漫长演化,既相对稳定、动态平衡,又相互作用、不断变化,各圈层之间的物质和能量不停循环,这些循环既跟物质的组成、结构和性质有关,也受人类活动的影响,并通过复杂的物理变化和化学变化实现。

(一)内涵决定身份﹣﹣物质的组成与分类
(l)用化学符号填空:
岩石圈中含量最高的金属元素是_____。大气圈中含量最高的物质是_____。水圈中含量最高的元素是_____。土壤中能促进农作物根系发达的元素是_____。
(2)按要求填表:
物质所属圈层 | 物质名称 | 物质的化学式 | 用符号表示构成物质的微粒 | 物质类别 |
生物圈 | 蔗糖 | _______ | _______ | _______ |
大气圈 | 氩气 | _______ | _______ | _______ |
水圈 | 氢氧化钙 | _______ | _______ | _______ |
岩石圈 | _______ | _______ | Na+、SiO32﹣ | _______ |
(二)甲烷﹣﹣小分子,大作为
在如图的四大圈层中,有下列6种物质:①甲烷;②水;③二氯化碳;④一氧化碳;⑤氢气;⑥氧气。构成这些物质的分子虽然简单,但这些物质有的是人类赖以生存的基本物质,有的是物质循环关键物质,有的是人类社会生产活动必需的物质。请回答:
(1)在这6种物质中,元素种类共有_____种,人类的生命活动不可缺少的物质有_____(填化学式,下同),植物生长必需的物质有_____,元素种类完全相同的物质是_____。
(2)甲烷是最重要的基础有机物之一,不仅可做燃料,还能发生如下反应:
①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②~④三个反应的化学方程式:
②_____;
③_____;
④_____;
(3)在反应①~④中,属于置换反应的有_____。
在反应①和②中,反应物相同,而生成物不同,从微观的角度看,是因为反应条件不同导致_____。
③和④两个反应的反应物不同,但生成物相同,从物质组成的角度看,其原因是_____。
在实际生产中,反应③需要按比例控制氧气不能超量,从物质性质的角度看,原因是_____。
(三)柔之力﹣﹣神奇的水溶液
水在生活、生产和科学实验中应用广泛。岩石圈约有四分之三被水覆盖,其中的某些物质被水溶解,其随水的天然循环在水圈中富集,富集后的物质可能再次沉积到岩石圈。
如图是氯化钠和碳酸钠的溶解度曲线。据图回答下列问题:
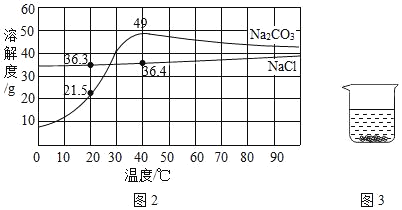
(1)青海湖区的人们有一种经验,冬天捞“碱”、夏天晒盐,这里的“碱”指纯碱,盐指氯化钠,他们所依据的原理是____。
(2)纯碱是一种重要的化工原料,但仅用物理方法从盐湖中“捞碱”远远不能满足需求,工业上主要利用从水圈中获得的食盐来制备纯碱,其反应的化学方程式是_____、_____。
(3)为确定某白色固体是碳酸钠还是氯化钠,在20℃时,取2.5g样品加入盛有10g水的烧杯中,充分搅拌后现象如图所示,则固体粉末是_____。若将该溶液升温到40℃时,则所得溶液溶质质量分数为_____。
(四)金属﹣﹣工业的脊梁
金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制'备金属镁,流程如图所示:
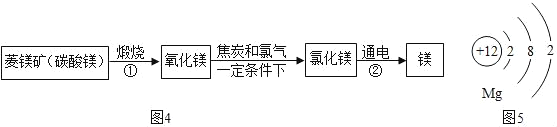
请回答下列问题:
(l)已知①和②属于分解反应,化学方程式分别为_____和_____。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明(用化学方程式表示其制备原理)_____。
(3)如图是镁原子结构示意图,镁化学性质活泼,原因是_____。四大圈层中含有下列物质:①硫酸锌;②氯化钠;③硫酸;④氢氧化钙;⑤氧气。其中能和铁反应的物质有(填序号)_____。
(4)小梅同学将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,她认为这种黑色物质是碳单质。在上述过程中,小梅运用的科学方法有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题.他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验 一 | 将氯酸钾加热至融化,伸入带火星的木条 | 木条复燃 | 氯酸钾受热分解产生氧气,但____________, 反应的文字表达式:___________________ | 二氧化锰是氯酸钾 受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条 | 木条不复燃 | 二氧化锰受热不产生氧气 | |
实验三 | ____________ | 木条迅速复燃 | 二氧化锰能加快氯酸钾的分解 | |
(1)请你帮助小明同学填写上表中未填完的空格;
(2)在小明的探究实验中,实验一和实验二起的作用是_____;
(3)小英同学认为仅由上述实验不能完全得出表内“总结”,她补充设计了 两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是_____;
第二方面的实验是要_____(写实验目的).
第二方面的实验目的已经明确,如何设计实验加以证明?请写出实验步骤,现象,结论:
步骤:_____.
现象:_____.
结论:_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com