
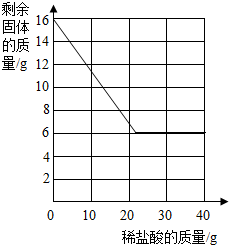
 某研究性学习小组的同学前往当地的大理石进行调査,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测.采用了以下的办法:取16g这种大理石,逐滴滴加稀盐酸,剩余固体的质量与所加盐酸的质量关系如图示(杂质不溶于水,不与盐酸反应).
某研究性学习小组的同学前往当地的大理石进行调査,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测.采用了以下的办法:取16g这种大理石,逐滴滴加稀盐酸,剩余固体的质量与所加盐酸的质量关系如图示(杂质不溶于水,不与盐酸反应).分析 由图中信息可知大理石中杂质质量是6g,碳酸钙和稀盐酸恰好完全反应时消耗稀盐酸质量是24g;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解:(1)大理石中的碳酸钙的质量是:16g-6g=10g,
答:大理石中碳酸钙质量是10g.
(2)设24g稀盐酸中氯化氢质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73
10g x
$\frac{100}{10g}$=$\frac{73}{x}$,
x=7.3g,
盐酸中溶质的质量分数为:$\frac{7.3g}{24g}$×100%=30.4%,
答:盐酸中溶质的质量分数为30.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
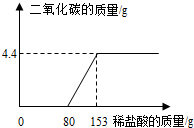 某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示.试计算:
某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题

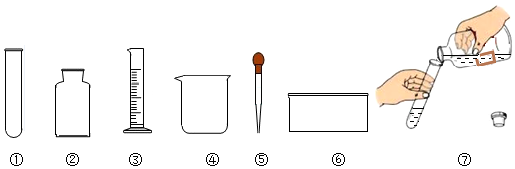
| A. | ①④⑥ | B. | ①④⑤ | C. | ①②④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
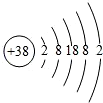 据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:
据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放.
使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
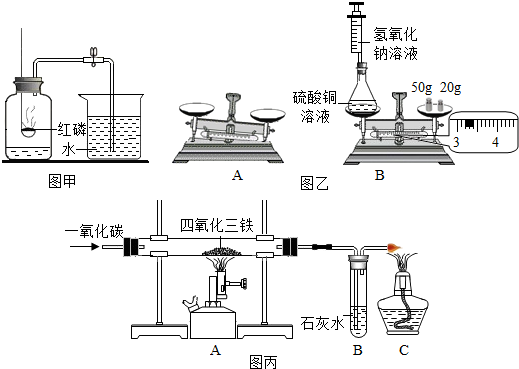
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
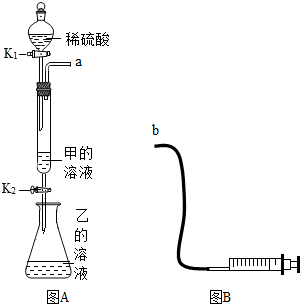
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com