
 如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.
如图是初中化学中常见物质间的转化关系,图中“→”表示转化关系,“-”表示相互能反应,反应条件间和部分物质已省略.已知A是胃酸的主要成分,D可用于配置波尔多液,其中A+B→C+F+G,A+N→C+F+G,请回答下列问题.分析 根据题目中的突破口“A是胃酸的主要成分”,可推测A为稀盐酸;根据“D可用于配置波尔多液”,可推测D为硫酸铜或氢氧化钙,根据“A+B→C+F+G,A+N→C+F+G”,结合图框,可推测D只能为氢氧化钙,则推测A与碳酸钠、碳酸氢钠反应,依次为突破口,结合图框,可推测:A为稀盐酸,B为碳酸氢钠,C为氯化钠,D为氢氧化钙,E为氢氧化钠,F为为水,G为二氧化碳,M为碳酸钙,N为碳酸钠.带入检验,符合题意.
解答 解:
根据题目中的突破口“A是胃酸的主要成分”,可推测A为稀盐酸;根据“D可用于配置波尔多液”,可推测D为硫酸铜或氢氧化钙,根据“A+B→C+F+G,A+N→C+F+G”,结合图框,可推测D只能为氢氧化钙,则推测A与碳酸钠、碳酸氢钠反应,依次为突破口,结合图框,可推测:A为稀盐酸,B为碳酸氢钠,C为氯化钠,D为氢氧化钙,E为氢氧化钠,F为为水,G为二氧化碳,M为碳酸钙,N为碳酸钠.带入检验,符合题意.
(1)根据分析,A的化学式为HCl;N的一种用途制取洗涤剂、制玻璃的原料;
(2)根据分析,D→E即氢氧化钙与碳酸钠溶液反应,其化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)根据分析,A-N即稀盐酸与碳酸钙反应,其化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:
(1)HCl;制取洗涤剂、制玻璃的原料;(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;(3)CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
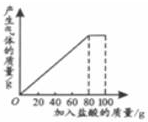 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | 第7次 | 第8次 | |
| 稀硫酸的质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 生成气体的质量/g | 0 | 0 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活垃圾焚烧产生的有害气体 | B. | 建筑施工导致尘土飞扬 | ||
| C. | 生物腐烂放出的一氧化碳 | D. | 煤燃烧产生的刺激性气味气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精 乙醇 C2H5OH | B. | 纯碱 氢氧化钠 NaOH | ||
| C. | 熟石灰 氧化钙 Ca0 | D. | 干冰 水 H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com