
| A. | 托盘天平、烧杯、玻璃棒 | B. | 量筒、托盘天平、烧杯 | ||
| C. | 量筒、烧杯、玻璃棒 | D. | 量筒、玻璃棒 |
分析 20%的硫酸50g,把它配成10%的硫酸,采用的是加水稀释的方法,其操作步骤是计算、量取、溶解,据此判断所需的仪器.
解答 解:A、用20%的硫酸50g配成10%的硫酸,其操作步骤是计算、量取、溶解,量筒用于量取浓硫酸和水,烧杯、玻璃棒用于进行溶解操作,无需使用托盘天平,故选项错误.
B、用20%的硫酸50g配成10%的硫酸,其操作步骤是计算、量取、溶解,量筒用于量取浓硫酸和水,烧杯、玻璃棒用于进行溶解操作,无需使用托盘天平,故选项错误.
C、用20%的硫酸50g配成10%的硫酸,其操作步骤是计算、量取、溶解,量筒和胶头滴管用于量取浓盐酸和水,烧杯、玻璃棒用于进行溶解操作,故选项正确.
D、用20%的硫酸50g配成10%的硫酸,其操作步骤是计算、量取、溶解,该选项缺少烧杯,故选项错误.
故选:C.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 滴有酚酞的氢氧化钠溶液中,继续滴加稀盐酸,红色消失,通过证明反应物的消失证明反应的发生 | |
| B. | 在无色溶液中滴入酚酞试液,溶液变红色--该溶液一定是碱性溶液 | |
| C. | 向氢氧化钠溶液与二氧化碳反应的生成物中,加足量稀盐酸有气泡冒出,通过证明生成物的存在证明反应的发生 | |
| D. | 向制取二氧化碳后的溶液中加入碳酸钠,开始没有沉淀产生,过一会有沉淀产生,说明溶液中可能存在少量盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 汽油挥发 光合作用 | B. | 煤气燃烧 石油蒸馏 | ||
| C. | 风力发电 木炭吸附 | D. | 海水晒盐 干冰升华 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
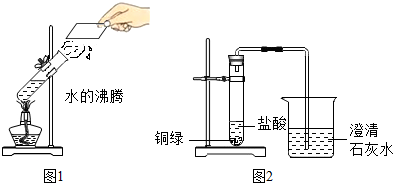
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20%的蔗糖溶液 | |
| B. | 把40g蔗糖全部溶解在210g水中所配成的溶液 | |
| C. | 150g溶液中含有27g蔗糖 | |
| D. | 把xg水加入到xg30%的蔗糖溶液中 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
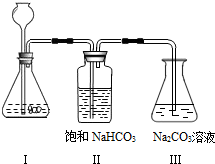
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com