
分析 (1)从金属的防腐、回收再利用及开采和寻找新的代替品这些方面去考虑;
(2)发热剂需要接触空气才会发热,原因是铁要与水、氧气等物质共同作用才会生锈;
(3)焦炭的作用:提供热量、生成一氧化碳;在炼铁中石灰石起作用是将矿石中的二氧化硅等杂质转变为炉渣而除去.
(4)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,可以使用铜盐溶液和银或银盐溶液和铜来进行证明;
(5)根据三种金属的活动性强弱关系(锌>铁>铜),分析可能发生的反应,判断溶液中含有的溶质以及滤出的金属固体.
(6)剩余固体是铜,由铜和混合物的质量可以计算出混合物中铜的质量分数和锌的质量;由锌和稀硫酸的质量根据锌和硫酸反应的化学方程式可以计算出稀硫酸的溶质质量分数
解答 解:(1)保护金属资源可以从防止金属锈蚀、回收废旧金属、合理开采金属资源和寻找金属代用品的角度进行,
(2)发热剂需要接触空气才会发热,原因是铁要与水、氧气等物质共同作用才会生锈;
(3)焦炭的作用:提供热量、生成一氧化碳;在炼铁中石灰石起作用是将矿石中的二氧化硅等杂质转变为炉渣而除去.
(4)A、铜和银都不与盐酸反应,无法确定二者的强弱,故A错误;
B、铜和银都不与硫酸反应,无法确定二者的强弱,故B错误;
C、铜和银都不与硫酸锌反应,无法确定二者的强弱,故C错误;
D、铜能与硝酸汞反应置换出银白色的汞,说明铜在汞前,而银不与硝酸汞反应,说明汞在银前,能比较得出铜和银的强弱,故D正确,
故选D;
(5)根据三种金属的活动性强弱关系(锌>铁>铜)可知:首先锌和氯化铜溶液反应,置换出单质铜;如果锌足量可以再继续和氯化亚铁反应置换出铁;向滤出的固体中滴加稀盐酸,有少量气泡产生,说明固体中含有与稀盐酸反应的金属.但不能确定和盐酸反应的是铁还是铁和锌的混合物,所以得到的金属一定有铜、铁,可能含有锌.滤液中一定没有CuCl2,因为固体中含有和盐酸反应的金属,说明CuCl2中的铜全部被置换出来了;滤液中一定含有生成的ZnCl2,无法确定是否含有氯化亚铁.
故答案为:Cu、Fe;CuCl2
(6)①混合物中铜的质量分数为$\frac{3.5g}{10.0g}$×100%=35%
②设稀硫酸中溶质的质量分数为x.
Zn+H2SO4=ZnSO4+H2↑
65 98
10.0g-3.5g 49.0g•x
$\frac{65}{10.0g-3.5g}$=$\frac{98}{49.0g•x}$,
x=20%
故答案为:(1)防止金属锈蚀;
(2)水、氧气
(3)提供热量、生成一氧化碳;将矿石中的二氧化硅等杂质转变为炉渣而除去.
(4)D
(5)Cu、Fe;CuCl2
(6)①混合物中铜的质量分数为35%.
②稀硫酸中溶质的质量分数为20%
点评 本题主要考查金属资源保护、铁生锈的条件和化学方程式的书写等,要加强记忆有关的知识点,并理解应用.本考点基础性强,比较好把握


 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:初中化学 来源: 题型:解答题
 如图是某品牌补铁剂的标签.请回答:
如图是某品牌补铁剂的标签.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 ,下列有关钙的判断错误的是( )
,下列有关钙的判断错误的是( )| A. | Ca元素位于周期表中的第4周期ⅡA族 | |
| B. | 钙原子核内质子数n为40 | |
| C. | 钙原子核外有20个电子 | |
| D. | 人体所补钙元素为金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是某同学正在绘制的实验室用一种药品制取氧气的装置图.请回答:
如图是某同学正在绘制的实验室用一种药品制取氧气的装置图.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu(Fe):可将混合粉末加入到足量硫酸铜溶液中,充分反应后过滤 | |
| B. | FeCl2(CuCl2):可往混合液中加入过量铁粉、充分反应后过滤 | |
| C. | CO(CO2):可将混合气体通过盛有足量澄清石灰水溶液的洗气瓶 | |
| D. | NaCl(Na2CO3):可往混合液中加入适量Ca(OH)2溶液,完全反应后过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
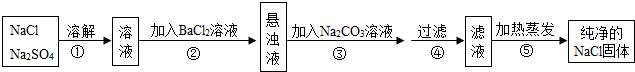
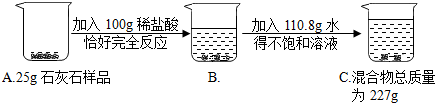
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②④ | D. | ②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com