
【题目】下列是与铁的性质有关的部分实验图,请回答下列问题。
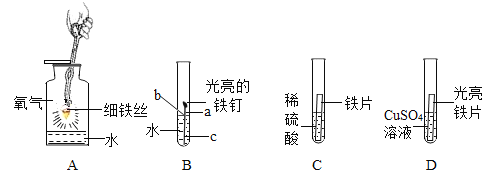
(1)A中发生化学反应生成的黑色固体的化学式为_____________。
(2)B中铁钉最易生锈的部位是_____________(填“a”、“b”或“c”)。
(3)C试管内发生的化学反应的化学方程式是_________________。
(4)D中反应一段时间后,若反应后铁片有剩余,则溶液中一定存在的金属阳离子为_________.
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】我国海洋资源丰富,开发前景十分远大。从海洋中提取的金属镁可以广泛应用于生活、生产和国防工业。
(1)从海水中提取单质镁的过程如下图所示:
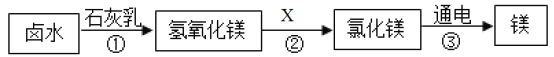
Ⅰ.写出上述转化过程①中,氯化镁溶液与石灰乳发生反应的化学方程式_________。
Ⅱ.过程②中加入的试剂X的名称为__________.
(2)某化学兴趣小组对一份MgCl2和Mg(OH)2的混合粉末展开了探究。取10 gMgCl2和Mg(OH)2的固体混合物于烧杯中,向其中逐滴加入溶质质量分数为10%的稀盐酸,烧杯中固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:
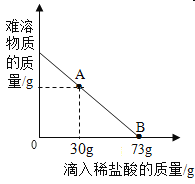
Ⅰ.在滴入稀盐酸的过程中,观察到的明显实验现象________。
Ⅱ.当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)_________。
Ⅲ.当滴入10%的稀盐酸73g时(即B点),试通过计算,求此时所得不饱和溶液中溶质的质量________。(计算结果精确到0.lg)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某微型实验的装置图。
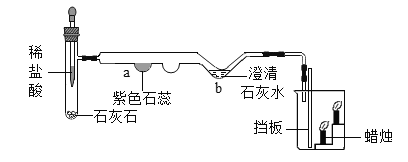
(1)反应发生后,a处现象为_____,烧杯内现象为_____。
(2)b处发生的化学方程式为_____。
(3)若用酒精灯对反应后的a处加热,则现象为_____。
(4)为测定某石灰石样品中碳酸钙的质量分数,称取10 g 石灰石(杂质不参加反应)放入烧杯中,加入100 g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7 g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年诺贝尔化学奖给了锂电池:没有他们,你的手机就是个点燃的炸药包,锂在化合物中显+1价。如图A是锂元素在周期表中的一些信息。图B~E是四种粒子的结构示意图,图F是一种粒子模型。
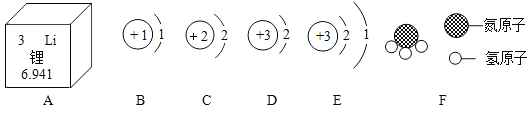
(1)从图1中A可获得锂元素的相对原子质量为___________。
(2)B、C、D、E中,属于同种元素的是_______________。(填序号)
(3)F所表示物质的化学式为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分仪器或装置如下图所示,请回答下列问题。
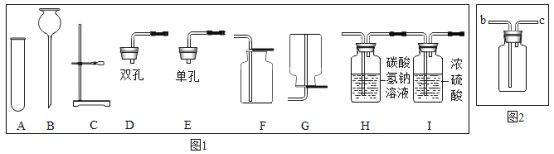
(1)写出仪器B的名称____________。
(2)实验室以氯酸钾为原料制取并收集氧气,完成这个实验图1中还缺少的仪器是_______,反应的化学方程式为____________。若用图2的装置收集氧气,氧气从_______导管口通入(填“b”或“c”),验满的方法__________。
(3)在实验室制取并收集一瓶纯净干燥的二氧化碳,请从图1中选择合适的仪器组装,装置组合为____和H(填编号),反应的化学方程式为________________ , 该反应的基本反应类型_________。其中H装置中碳酸氢钠溶液的作用是__________________。
(4)为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。
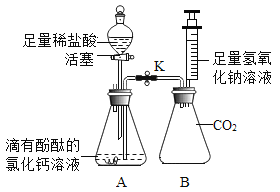
实验一:氢氧化钙溶液与稀盐酸发生反应
打开分液漏斗的活塞,使稀盐酸逐滴滴加入A中锥形瓶,观察到___________的现象时,关闭活塞,证明氢氧化钙溶液与稀盐酸发生反应;
实验二:氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入B中锥形瓶,过一段时间后,打开弹簧夹K,观察到_________的现象并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是_____________。锥形瓶B中溶液最后呈红色_________(填“能”或“不能”)证明氢氧化钠有剩余。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年来一些手机厂商纷纷发布自己的可折叠手机。化学物质吡唑啉是生产折叠手机用到的柔性屏幕的重要物质,其化学式为C3H6N2,下列有关吡唑啉C3H6N2的说法正确的是( )
A.吡唑啉属于氧化物
B.吡唑啉是由3个碳原子、6个氢原子和2个氮原子构成的
C.吡唑啉中碳元素质量分数最大
D.吡唑啉的相对分子质量为70g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“共享单车”是指在公共场所提供共享服务的自行车,由于符合“低碳出行”的理念,颇受年轻人的喜爱。

(1)“低碳出行”中“低碳”指的是较低的_________气体排放;
(2)上图所示自行车中的材料属于金属材料的是________(选填一个序号,下同),属于有机合成材料的是_________;
(3)钢丝制成的网篓抗腐蚀性能较好,请用一个化学方程式表示铝和铁的活动性强弱:____;
(4)从当初发展经济大量使周“化石燃料”,到今天的“低碳出行”,谈谈你的感受:_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌纯碱中含有少量氯化钠。某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。
(一)甲组同学设计如图1所示实验:
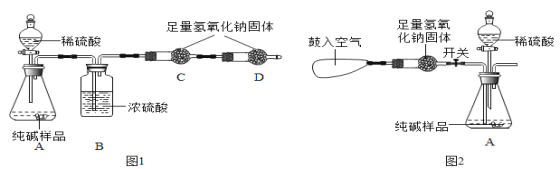
(实验步骤)
①组装好如图仪器,并检查装置的气密性;
②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C的总质量;
⑥计算出样品中碳酸钠的质量分数。
(实验分析)
(1)A装置中反应的化学方程式为_____。
(2)B装置的作用是_____。
(3)如果没有B装置则所测样品中碳酸钠的质量分数_____(填偏大、偏小、不变);
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是_____。
(5)按以上实验步骤,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为_____%(精确到0.1%)。
(二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:
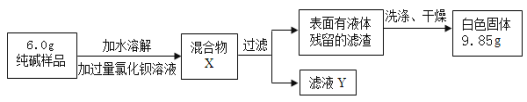
(1)判断加入氯化钡溶液是否过量的合适方法是_____,然后观察现象判断。
A 静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量;
B 向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量。
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加_____,然后观察现象判断。
A 氯化钡溶液 B 稀硫酸 C 硝酸银溶液 D 稀盐酸
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为_____%(写出具体计算过程,结果精确到0.1%)。
(实验反思)
丙组同学认为若使用图1装置会使测得的碳酸钠的质量分数_____(填“偏大”、“偏小”、或“无法判断” )为了克服图1装置的不足,有同学提出把A装置作如图2的改进(A装置中原双孔橡胶塞换成三孔橡胶塞),在反应前、后用图2装置分两次缓缓鼓入空气。反应后,用图2装置鼓入空气的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
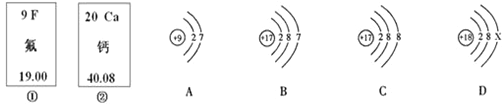
(1) 氟原子的核电荷数为____________,
(2) 钙元素的相对原子质量为________;
(3) A、B、C、D中属于同种元素的粒子是_____________(填序号);
(4) A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_______(填序号);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com