
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

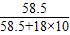 ×100%=25%.
×100%=25%.

科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:
化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化.
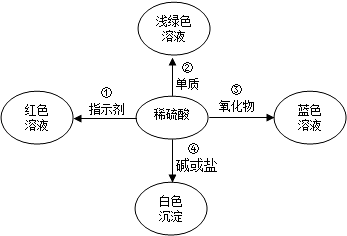
(1)请你在编号②、③处各填入一种物质.②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质.请你写出编号①稀硫酸的化学性质 .
(3)若编号④的物质是盐.请你写出符合编号④的一个化学方程式: ,反应类型是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
化学使世界变得绚丽多彩.如图是物质之间发生化学反应的颜色变化.

(1)请你在编号②、③处各填入一种物质.②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质.请你写出编号①稀硫酸的化学性质 .
(3)若编号④的物质是盐.请你写出符合编号④的一个化学方程式: ,反应类型是
查看答案和解析>>
科目:初中化学 来源:2013年广东省湛江市中考化学试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com