
 2MgO;化合.
2MgO;化合. 2MgO
2MgO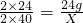 ,解得X=40g
,解得X=40g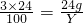 ,
,

科目:初中化学 来源: 题型:
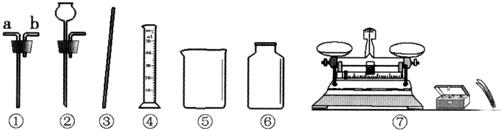
查看答案和解析>>
科目:初中化学 来源: 题型:
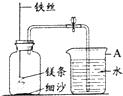 12、某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
12、某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.查看答案和解析>>
科目:初中化学 来源: 题型:
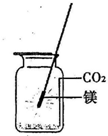 镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是
镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com