
【题目】KNO3 和 KCl 在不同温度时的溶解度如表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
(1)依据上表数据,绘制 KNO3 和 KCl 的溶解度曲线,如图 1 中能表示 KNO3 溶解度曲线的是_____(填 m 或 n)。
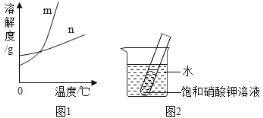
(2)20 ℃时,向 10 g 水中加入 2.5 g KNO3 充分搅拌得到 X,再加入 2.5 g KNO3 充分搅拌得到 Y,继续升温至 50 ℃得到 Z,则 X、Y、Z 中为饱和溶液的是_____。
(3)40 ℃时,100 g 水中的硝酸钾饱和溶液稀释成溶质质量分数为10%的溶液,应加水的质量为_____。
(4)如图 2 所示,20 ℃时,将盛有饱和 KNO3 溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____(填字母序号)。
A. 硝酸铵固体 B. 生石灰固体 C. 冰块
(5)将40℃时硝酸钾和氯化钾的饱和溶液,降温至10
A. KNO3溶液析出晶体的质量比KCl析出晶体的质量大
B. 在20℃和30℃之间某一温度,两种溶液的质量分数相等
C. 两种溶液的溶剂质量不变
D. 若继续对两溶液降温,则两溶液将会继续析出晶体,且水溶液会成为纯净物
【答案】m Y 475.1g AC BC
【解析】
(1)根据表格中数据可知,硝酸钾的溶解度受温度影响较明显,所以图 1 中能表示KNO3 溶解度曲线的是m。故填:m。
(3)20 ℃时,硝酸钾的溶解度为31.6g,即100g水中可以溶解31.6g硝酸钾达到饱和,所以 10 g水中最多可以溶解3.16g硝酸钾,向10g水中加入 2.5 g KNO3 充分搅拌得到 X为不饱和溶液,再加入 2.5 g KNO3 ,一共加入了5g硝酸钾,不能全部溶解,所以充分搅拌得到 Y是饱和溶液,继续升温至 50 ℃,该温度下硝酸钾的溶解度为85.5g,100g水中最多溶解85.5g达到饱和,10g水中可以溶解8.55g达到饱和,但是加入的硝酸钾只有5.0g,所以得到的Z为不饱和溶液,所以则X、Y、Z 中为饱和溶液的是Y。故填:Y。
(3)40 ℃时,100 g 水中的硝酸钾的饱和溶液(含溶质63.9g)稀释成溶质质量分数为10%的溶液,稀释后稀溶液的质量为![]() ,原溶液的质量为
,原溶液的质量为![]() ,所以应加水的质量为
,所以应加水的质量为![]() 。故填:475.1g。
。故填:475.1g。
(4)如图 2 所示,20 ℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,温度降低会导致饱和硝酸钾溶液溶解度减小而析出晶体,所以加入的物质会导致溶液温度降低,符合题意的是A 硝酸铵固体(它溶解吸热,使溶液温度降低)或者C冰块(它要融化吸热,使溶液温度降低),但是B生石灰遇水反应放热,会使溶液温度升高,硝酸钾不会析出晶体。故选AC。
(5)A. 因为没有指明饱和硝酸钾溶液和饱和氯化钾溶液的质量是否相等,所以KNO3溶液析出晶体的质量与 KCl 析出晶体的质量无法比较。故A不符合题意;
B. 因为在20℃时氯化钾的溶解度大于硝酸钾的溶解度,在30℃时硝酸钾的溶解度大于氯化钾的溶解度,所以二者溶解度相等的温度点出现在20℃和30℃之间某一温度,将40℃时硝酸钾和氯化钾的饱和溶液,降温至 10℃,降温过程溶液始终饱和,当溶解度相等时两种溶液的质量分数相等为![]() 。故B符合题意;
。故B符合题意;
C. 将40℃时硝酸钾和氯化钾的饱和溶液,降温至 10℃,降温过程两种溶液只是会析出晶体,溶剂的质量不变。故C符合题意;
D. 若继续对两溶液降温,则两溶液将会继续析出晶体,但是水溶液不会成为纯净物,还会有少量晶体溶解在水中,溶液属于混合物。故D不符合题意。
故选BC。


 高中必刷题系列答案
高中必刷题系列答案科目:初中化学 来源: 题型:
【题目】2020年,新型冠状病毒在全球肆虐,做好个人防护是抗击“新冠”疫情的有效方法,口罩、84消毒液、医用酒精是居家“抗疫”的常见物品(如图)。
(1)医用外科口罩可以阻挡70%的微细颗粒,能满足一般防护需要,制作材料主要是聚丙烯。聚丙烯属于_____。
A 单质 B 无机物 C 天然高分子材料 D 合成高分子材料
(2)84消毒液是次氯酸钠(NaClO) 为主要成分的水溶液。次氯酸钠在水中可产生次氯酸,次氯酸具有强氧化性,可有效杀灭细菌和病毒。次氯酸钠中氯元素的化合价为_____,次氯酸的化学式为_____。84消毒液不能与洁厕灵(主要成分为盐酸)混合使用,原因是:次氯酸钠和盐酸混合反应,产生氯化钠、氯气(Cl2)和水,而氯气是一种有毒气体。该反应的化学方程式为:_____。
(3)医用酒精是浓度为75%的乙醇(C2H5OH)溶液,能有效杀灭新冠病毒,具有可燃性。下列说法正确的是_____(填序号)。
A 乙醇属于有机化合物
B 医用酒精的溶质是水,溶剂是乙醇
C 可以大量携带医用酒精搭乘公交地铁
D 使用医用酒精消毒时,应该远离火源
(4)学校现有30kg溶质质量分数为95%的高浓度酒精,要稀释成75%的医用酒精,需要蒸馏水_____kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年2月5日长征五号B遥——火箭运抵海南文昌航天发射场,4月中下旬执行首次发射任务。请结合所学知识回答有关问题:
(1)制造火箭使用了铝合金、钛合金、聚四氟乙烯、聚氨酯橡胶、新型陶瓷等材料,其中属于合成高分子材料的是_______。
(2)钛合金常用于制火箭外壳,钛冶炼时有如下反应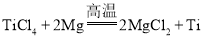 ,该反应需要在氩气中进行,所利用的氩气的性质主要是______。
,该反应需要在氩气中进行,所利用的氩气的性质主要是______。
(3)长征五号B遥——火箭采用液氧、液氢和煤油作为推进剂。
①工业上常用分离液态空气方法制取氧气,该过程发生的变化属于____ ( 填“物理”或“化学”)变化。
②工业上可用下列反应制取氢气: Ⅰ. 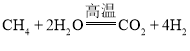 、Ⅱ
、Ⅱ 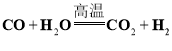 .
.
反应Ⅰ中表现出还原性的物质是___。
③若用C14H30表示煤油,煤油完全燃烧的化学方程式为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下图是利用海水提取粗盐的过程:
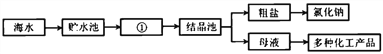
上图中①是_____池 (填“蒸发”或“冷却”)。
(2)粗盐中含有少量 CaCl2、MgCl2、Na2SO4 和泥沙,某同学将该粗盐样品进行提纯。
①将样品加适量水溶解,然后进行_____,除去泥沙等难溶性杂质,得到澄清溶液;
②向所得的澄清溶液中依次加入稍过量的 BaCl2 溶液、NaOH 溶液和_____溶液, 除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯挣的 NaCl 溶液;
③蒸发溶液,得到较多氯化钠固体时停止加热,他注意到不能立即把_____直接放 在实验台上,以免烫坏实验台。
(3)另一同学用所得的氯化钠和蒸馏水配制溶质质量分数为 6%的氯化钠溶液。配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。配制上述溶液的正确顺序是_______ (填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是自然界中碳、氧循环简图(X为H2CO3,Y为C6H12O6)。下列说法不正确的是
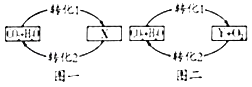
A. 图一中的转化1是酸雨形成的主要原因
B. 图二中可实现有机物与无机物的相互转化
C. 绿色植物通过光合作用,将太阳能转化成化学能
D. 碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回顾实验室制取![]() 的实验,我们可知:研究实验室制取气体的一般顺序:
的实验,我们可知:研究实验室制取气体的一般顺序:
(1)首先研究生成该气体的化学反应原理;
(2)然后根据反应物的状态和反应的条件选择并安装实验仪器,而且一定要检查________;
(3)根据收集气体的________和________确定气体的收集方法;
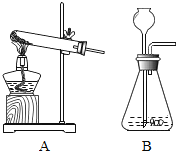
(4)图中是制氧气的两套装置,按要求回答:
①加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为________;制得氧气后,剩余固体是氯化钾(易溶于水)和二氧化锰(难溶于水)的混合物,将它们分离后可回收使用.分离时,先将混合物放在烧杯中,加适量________并________;将所得的悬浊液进行________,可得到________;将滤液进行________,可得到________.
②实验室用过氧化氢和二氧化锰制氧气可选________(图A或B),原因________.
③某兴趣小组取![]() 克过氧化氢溶液在
克过氧化氢溶液在![]() 克二氧化锰的作用下反应,反应一段时间后测得容器中剩余物质的总质量为
克二氧化锰的作用下反应,反应一段时间后测得容器中剩余物质的总质量为![]() 克.试计算:
克.试计算:
(A)该实验中生成氧气的质量为________克,物质的量________摩尔.
(B)根据化学方程式列式计算参加反应的过氧化氢的物质的量____________.
④硫化氢![]() 是一种具有臭鸡蛋气味的气体,其密度比空气的密度大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁
是一种具有臭鸡蛋气味的气体,其密度比空气的密度大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁![]() 和稀硫酸
和稀硫酸![]() 混合,在常温下发生反应生成硫酸亚铁和硫化氢气体.试回答:
混合,在常温下发生反应生成硫酸亚铁和硫化氢气体.试回答:
(A)实验室制取硫化氢的化学反应方程式为:________.
(B)制取硫化氢气体的发生装置可以选用________(图A或B);
(C)收集硫化氢气体可用________法.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳在地壳中的含量不高,但它的化合物数量众多,而且分布极广。根据所学知识回答:

(1)图①为碳原子的结构示意图,碳原子最外层电子数为________,常温下碳的化学性质________,(填“活泼”或“不活泼”)。
(2)图②、③、④对应三种碳单质:图②单质的名称是________,图③单质的名称是________,图④单质的化学式是________。
(3)C为+4价,Cl为-1价,由C和Cl组成的化合物的化学式为________。
(4)实验室若选用图⑤装置制取二氧化碳,则需要改正的一点是________,请你写出用石灰石与稀盐酸反应制取二氧化碳的化学方程式________,将产生的二氧化碳气体通入澄清石灰水,反应的化学方程式是________。
(5)用制取的二氧化碳进行如下实验:
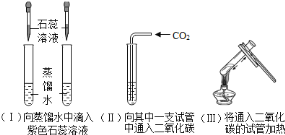
①实验(II)中溶液变________色。
②实脸(III)中加热之后溶液又变为________色,用化学方程式解释出现此现象的原因________。
(6)工业上高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳。如果要制取10t氧化钙,需要碳酸钙多少吨______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,用“W”型玻璃管进行微型实验。
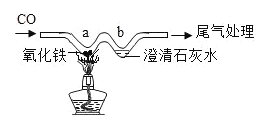
(1)描述a处的实验现象_____;
(2)写出b处发生反应的化学方程式_____。
(3)写出a处发生反应提供热量的化学反应方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下图溶解度曲线,判断下列说法错误的是( )
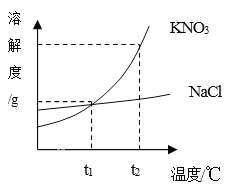
A. t2℃时,硝酸钾的溶解度为110g
B. 硝酸钾中含有少量氯化钠时,可以用冷却热饱和溶液的方法提纯硝酸钾
C. 将t2℃时硝酸钾的饱和溶液降温到t1℃,一定会析出(110-a)g晶体
D. t2℃时,等质量的两种物质的饱和溶液中,含硝酸钾的质量一定比含氯化钠的质量大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com