
【题目】(1)如图是某奶制品标签。请回答:
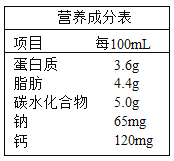
①“钠”指的是_____(填“单质”或“原子”或“元素)。
②人体每日必须摄入足量的钙,幼儿及青少年缺钙会患_____(填字母)和发育不良。
A 贫血 B 畸形、佝偻病
C 发育停滞、侏儒症 D 甲状腺疾病
(2)硒元素有防癌的作用。硒原子的结构示意图及硒元素在周期表中的信息如图所示。请回答下列问题。
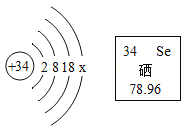
①硒元素的相对原子质量为_____。
②硒原子的核电荷数为_____,
在化学反应中硒原子容易_____(填“得到”或“失去”)电子。
(3)随着人类对能源的需求量日益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注。我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
①可燃冰主要含甲烷水合物,甲烷(CH4)完全燃烧的化学方程式为_____。
②氢气不便于贮存,可将其转化为固态氢化物(如氢化钠等)。氢化钠(NaH)与水反应生成氢氧化钠和氢气,该反应的化学方程式为_____。
【答案】元素 B 78.96 34 得到 CH4+2O2 2H2O+CO2 NaH+H2O=NaOH+H2↑
2H2O+CO2 NaH+H2O=NaOH+H2↑
【解析】
(1)①物质是由元素组成的,所以标签中的钠指的是元素;
②人体每日必须摄入足量的钙,幼儿及青少年缺钙会患畸形、佝偻病和发育不良。故选B。
(2)①根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,硒元素的相对原子质量为78.96。
②对于原子,原子序数=核内质子数=核电荷数=核外电子数,则硒原子的核电荷数为34;且 34=2+8+18+![]() ,
,![]() =6,即硒原子的最外层电子数为6,大于4,在化学反应中硒原子容易得到2个电子。
=6,即硒原子的最外层电子数为6,大于4,在化学反应中硒原子容易得到2个电子。
(3)①甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2 2H2O+CO2。
2H2O+CO2。
②氢化钠(NaH)与水反应生成氢氧化钠和氢气,该反应的化学方程式为NaH+H2O=NaOH+H2↑。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:
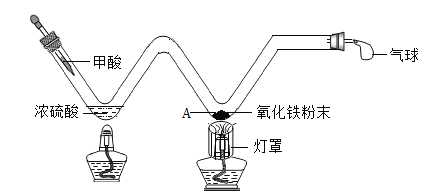
【题目】实验创新是重要的学科素养。小明用W形玻璃管完成了课本上的两个实验。
(1)探究炼铁原理如图:甲酸(HCOOH)在热的浓硫酸的作用下,分解生成一氧化碳和水,该反应的化学方程式是________,实验时,酒精灯加灯罩的作用是_________,A处可观察到的现象是__________。
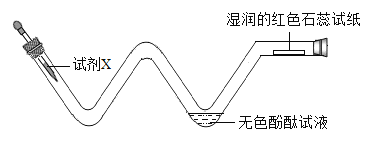
(2)探究微粒性质如图:加入试剂X,观察到无色酚酞试液变红,红色石蕊试纸变蓝。试剂X可能是______,该装置的优点是______(答一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化物会分解生成氧化物和氧气。
方法 1:由Ca(OH)2为原料最终反应制得,其制备流程如图:
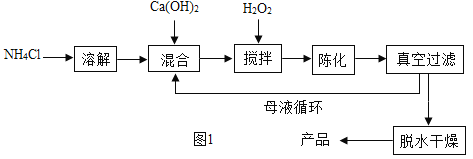
方法 2:由鸡蛋壳(含CaCO3高达 90%)为原料最终反应制得,其制备流程如图:
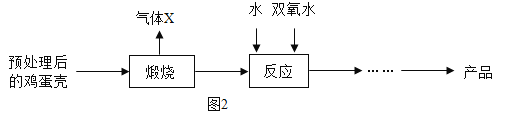
(1)方法 1 中搅拌的目的是_____。请将搅拌过程中发生反应的化学方程式补充完整![]() _____
_____![]() .制备过程中除水外可循环使用的物质是_____(填化学式)。
.制备过程中除水外可循环使用的物质是_____(填化学式)。
(2)方法 2 中气体 X 是_____,实验室常用_溶液来吸收。煅烧后的反应是化合反应,也能生成CaO28H2O,反应的化学方程式为_____。该反应需控制温度在 0~2℃,可将反应器放置在_,获得的CaO2产品中主要含有的固体杂质是_(填化学式)。
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能_____。
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO28H2O的反应符合“绿色化学”的是________(填“方法 1”或“方法 2”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:

(l)溴的相对原子质量是_______。
(2)溴元素的化学性质与图二哪种元素的化学性质相似_______(填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为:_______。
(4)若图二中C表示离子,则离子符号是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学欲运用所学知识和方法,分析某铁碳合金的组成。他们设计相关实验,并将实验过程用下图表述,请分析实验过程所给信息并结合计算回答以下问题: (钢的含碳量为0.03% ~2%,生铁的含碳量为2%~ 4.3%)
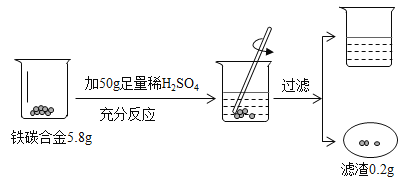
(1)铁碳合金属于 (填 “生铁”或“钢”)
(2)反应后烧杯中稀硫酸无剩余,请计算所用稀硫酸溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高阳同学通过阅读课外资料得知,潜水艇中常用过氧化钠(Na2O2)作为供氧剂,有关反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,2Na2O2+2H2O═4NaOH+O2↑。于是她用如图所的装置来制取CO2并验证其与Na2O2的反应。
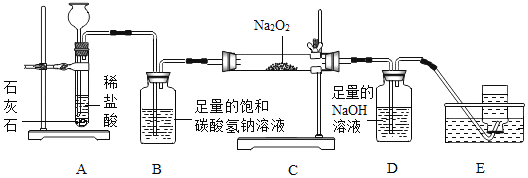
(1)装置B的作用是_____。
(2)反应一段时间后,装置E中收集到的气体主要是_____;反应后装置C硬质玻璃管中固体的成分是什么?高阳为此又进行了如下探究:
(猜想与假设)
猜想一 Na2CO3
猜想二Na2CO3和Na2O2
猜想三Na2CO3和NaOH
你认为还可能是_____
(设计实验)
实验操作 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的水,振荡 | 固体完全溶解,_____ | 样品中一定没有Na2O2 |
②取少量实验①所得溶液于另一试管中,加入过量的BaCl2溶液,振荡 | 有白色沉淀产生 | 猜想三正确 |
③取少量实验②所得上层清液于另一试管中,加入_____溶液,振荡 | 有白色沉淀产生 |
(反思与评价)反应后装置C硬质玻璃管中的固体含有NaOH,原因可能是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“太阳能光伏发电系统”在交通、通讯、海洋、气象、光伏电站、太阳能建筑等领域中,具有不同程度的应用。白天在太阳光照条件下,太阳能电池组件产生一定的电动势,对太阳能电池方阵中的蓄电池进行充电,将电能储存起来,晚上,将直流电转换成交流电,输送到配电柜进行供电。请回答下列问题:

(1)“太阳能光伏发电系统”在白天时工作过程中的能量转化是(用“→”表示转化)_____。
(2)该系统组成中的边框为铝合金制成,也是太阳能发电中最重要的部分,该材料具有抗机械冲击力好等性能,你认为该材料还应具备的物理性质是_____(填字母)。
A 密度小,抗腐蚀性好 B 熔点高,导电性好 C 强度高、密度小
(3)有科学家设想把太阳能光伏系统安装在家用车上,如果实现可以部分解决_____能源面临耗尽的问题,同时减少了_____等污染物的排放(填两种物质)。
(4)该系统组成的支架所用的钢材长时间使用后,需要对其表面进行处理,若用盐酸洗会产生“酸洗废液”(主要成分为FeCl2),工业上将“酸洗废液”在高温下与氧气、水反应制得氧化铁,同时产生氯化氢气体,写出此反应的化学方程式_____,反应前后铁元素的化合价分别为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是 a、b、c 三种物质的溶解度曲线。
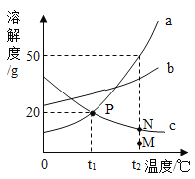
(1)点P表示__________;
(2)要使M点的c溶液变成N点的c溶液,可采取的一种措施是_____________;
(3)当a中含有少量的 b,要得到纯净的 a,可采用的方法是____________________;
(4)t2℃时,等质量的a、b、c三种物质的饱和溶液降温到t1℃时,三种溶液的质量分数由大到小的顺序______________;
(5)t2℃时,40ga物质加入到40g水中形成______g溶液。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图是配制80克质量分数为20的氯化钠溶液的操作过程示意图。试回答:
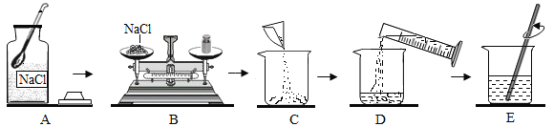
(1)B操作中应称量氯化钠的质量是__________,放好砝码和游码后,向托盘中加入氯化钠过程中,若指针偏向分度盘的左边,应进行的操作是__________。
(2)D操作应选用__________的量筒(从10mL、100mL中选择),量水时量筒必须平放,视线要与量筒凹液面的__________处保持水平。
(3)E操作的作用是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com