
| ||
| ||
| ||
| ||
| ||
| ||


科目:初中化学 来源: 题型:阅读理解
 “嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.
“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.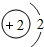 D.属于金属元素,在化学反应中易得到电子
D.属于金属元素,在化学反应中易得到电子
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1-2滴酚酞试液,变红后 加入过氧化氢溶液 加入过氧化氢溶液 观察现象 |
溶液依然为红色 | 不是生成的过氧化氢使溶液褪色 不是生成的过氧化氢使溶液褪色 |
| 实验步骤 | 实验现象 | 实验结论 |
取少量原溶液于试管中,加入适量水,观察现象 取少量原溶液于试管中,加入适量水,观察现象 |
(1)变回红色 (2)依然无色 (1)变回红色 (2)依然无色 |
(1)氢氧化钠溶液浓度过大导致溶液颜色褪去 (2)溶液颜色褪去与氢氧化钠溶液浓度无关 (1)氢氧化钠溶液浓度过大导致溶液颜色褪去 (2)溶液颜色褪去与氢氧化钠溶液浓度无关 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。
(1)为了安全和实验的成功,你必须要明确实验规则和实验的基本技能:
A.为了节约药品,用剩的药品应放回原试剂瓶
B.为了获得感性认识,可触摸药品或尝药品的味道
C. 为了安全,给试管里物质加热时,试管口不能朝着有人的方向
D. 为了能看清楚标签,倾倒试液时,标签不能向着手心
E.为了防止冷凝水回流,给试管中固体加热时,试管口略向下倾斜
以上认识和做法中不合理的有_________________________。
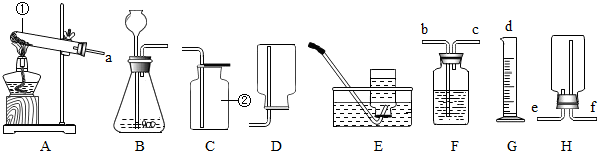
 (2)结合下列实验装置图回答问题:
(2)结合下列实验装置图回答问题:
⑴ 写出仪器①的名称
⑵ 实验室若用高锰酸钾为原料制氧气,则试管口应放 。收集氧气常选用E装置,是因为 __________ _____。若选择C装置收集氧气,则验满的方法是______ ______。
⑶ 实验室若选用B装置作为制取氧气的发生装置,则发生反应的文字(或符号)表达式为___________
若实验室用此法代替KMnO4制取O2,其优点是 (填编号,下同)。
A.操作简便 B.需加热 C.速度快
⑷氨气极易溶于水,且密度比空气小,实验室可用加热硫酸铵和熟石灰的固体混合物来制取氨气,制
取氨气的发生装置应选用 装置,若使用装置F收集氨气,则气体应从 ____(填“b” 或“c”)
通入。
⑸ F装置可以用来收集和储备气体。利用药品氯酸钾和装置A、F(装满水)、G可以制取氧气并测量氧气的体积,则接口的顺序为(填a、b、c、d):a→ → → 。当装置中收集满氧气后,如果需要排出氧气,则可使用水排法。水应从(填“b”或“c”) 端通入。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。
(1)为了安全和实验的成功,你必须要明确实验规则和实验的基本技能:
A.为了节约药品,用剩的药品应放回原试剂瓶
B.为了获得感性认识,可触摸药品或尝药品的味道
C. 为了安全,给试管里物质加热时,试管口不能朝着有人的方向
D. 为了能看清楚标签,倾倒试液时,标签不能向着手心
 E.为了防止冷凝水回流,给试管中固体加热时,试管口略向下倾斜
E.为了防止冷凝水回流,给试管中固体加热时,试管口略向下倾斜
以上认识和做法中不合理的有_________________________。
(2)结合下列实验装置图回答问题:
⑴ 写出仪器①的名称
⑵ 实验室若用高锰酸钾为原料制氧气,则试管口应放 。收集氧气常选用E装置,是因为 __________ _____。若选择C装置收集氧气,则验满的方法是______ ______。
⑶ 实验室若选用B装置作为制取氧气的发生装置,则发生反应的文字(或符号)表达式为___________
.若实验室用此法代替KMnO4制取O2,其优点是 (填编号,下同)。
A.操作简便 B.需加热 C.速度快
⑷氨气极易溶于水,且密度比空气小,实验室可用加热硫酸铵和熟石灰的固体混合物来制取氨气,制
取氨气的发生装置应选用 装置,若使用装置F收集氨气,则气体应从 ____(填“b” 或“c”)
通入。
⑸ F装置可以用来收集和储备气体。利用药品氯酸钾和装置A、F(装满水)、G可以制取氧气并测量氧气的体积,则接口的顺序为(填a、b、c、d):a→ → → 。当装置中收集满氧气后,如果需要排出氧气,则可使用水排法。水应从(填“b”或“c”) 端通入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com