
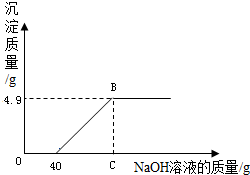
 (2011?营口) 现有硫酸和硫酸铜的混合溶液124.9g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀的质量与所加入的氢氧化钠溶液的质量关系如右图所示.求:
(2011?营口) 现有硫酸和硫酸铜的混合溶液124.9g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液直至生成Cu(OH)2沉淀,沉淀的质量与所加入的氢氧化钠溶液的质量关系如右图所示.求:| 溶质质量 |
| 溶液质量 |
| 80 |
| 98 |
| 10%x |
| 4.9g |
| 142 |
| 98 |
| y |
| 4.9g |
| 80 |
| 142 |
| 40×10%g |
| z |
| 7.1g+7.1g |
| 124.9g+40g+40g-4.9g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
(2011?营口)区分下列各组物质的两种方法都正确的是( )
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com