
在盛有40g溶质质量分数为20%氢氧化钠溶液的烧杯中,用滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中,验证“中和反应会放热”,同时用pH计记录溶液pH的变化,绘制成以下函数图像。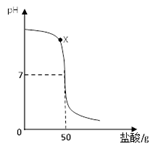
(1)用玻璃棒蘸取X点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有 。(填化学式)
(2)为什么不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”。 。
(3)当pH=7时,求溶液中溶质的质量分数。
(1)NaCl NaOH(2分,整体给分)
(2)氢氧化钠固体溶于水时也会产生热量,这样就无法说明热量来自于中和反应了(1分)
(3)13%(3分,计算出氯化钠质量1分,求出反应后溶液1分,计算出结果1分)
解析试题分析:(1)X点溶液的溶质中,含有氢氧化钠和稀盐酸反应生成的氯化钠及其没有反应的氢氧化钠;用玻璃棒蘸取X点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有氯化钠和氢氧化钠,化学式分别为NaCl、NaOH;
(2)因为氢氧化钠固体溶于水时也会放出热量,这样就无法说明热量来自于中和反应了,所以不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”;
(3)pH=7时,氢氧化钠和稀盐酸恰好完全反应,根据提供的数据可以计算溶液中溶质的质量分数:
设反应生成氯化钠的质量为x,
NaOH+HCl═NaCl+H2O,
40 58.5
40g×20% x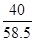 =
=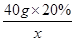
x=11.7g,溶液的质量为:40g+50g=90g,
当pH=7时,溶液中溶质的质量分数为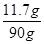 ×100%=13%.
×100%=13%.
答:当pH=7时,溶液中溶质的质量分数为13%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算


科目:初中化学 来源: 题型:计算题
(18分)硫酸亚铁铵晶体俗名为摩尔盐,化学式为xFeSO4·y(NH4)2SO4·zH2O,在制药、电镀方面有广泛的应用。
资料: ①硫酸亚铁铵晶体易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如下表:
| 温度/℃ | FeSO4 | (NH4) 2SO4 | xFeSO4·y(NH4)2SO4·zH2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21. 6 |
| 30 | 32.9 | 78 | 28.1 |



查看答案和解析>>
科目:初中化学 来源: 题型:计算题
过氧化钠是常用的供氧剂,可将CO2转化为O2,其反应的化学方程式是:2Na2O2 + 2CO2=2Na2CO3 + O2。若有22g CO2参加反应,计算生成O2的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我市锰矿资源丰富,MnO2是一种无机功能材料,主要用于制造干电池。当地某工厂加工得到了粗MnO2(主要含有杂质MnCO3,其它杂质忽略不计),为了测定其中MnO2的含量,称取57.5g粗MnO2样品,加入足量的稀硫酸溶液,产生CO2气体4.4g。
(已知:MnCO3+ H2SO4  MnSO4+H2O+CO2↑)
MnSO4+H2O+CO2↑)
试完成下列问题:(1)计算57.5g粗MnO2中含有MnCO3的质量,
(2)计算粗MnO2中的MnO2的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题: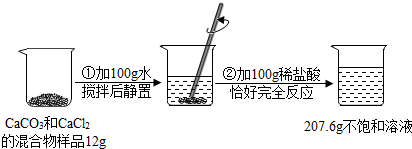
(1)实验所用稀盐酸的溶质的质量分数为 7.3%.
(2)计算原混合物样品中CaCl2的质量(写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6分)为测定Cu一Zn合金的组成,小华同学利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关实验数据记录如下:
| | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 1O | 10 | 20 |
| 加入硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室里可用锌与稀硫酸反应制取氢气:
Zn + H2SO4 = ZnSO4 + H2↑
某实验需要氢气2.24L。
(1)求参加反应的锌的质量。
(2)某兴趣小组用的是从废旧电池中得到的含杂质10%的锌皮制取氢气。现有这种废锌皮15g,与足量稀硫酸反应,最多得到氢气多少g?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
长期使用的水壶底部结有一层水垢,其主要成分是碳酸钙和氢氧化镁,为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用如图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表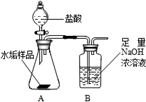
| | 第一次 | 第二次 | 第三次 | 平均值 |
| B装置增加的质量 | 2.17 | 2.22 | 2.21 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com