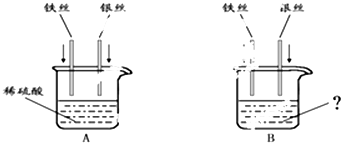
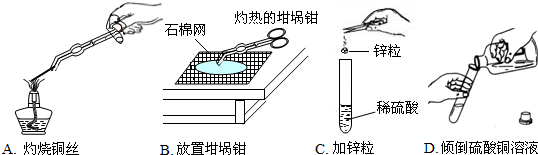
解:(1)①从实验室拿出来的铁丝和银丝表面是被空气中的氧气氧化过的,所以应该用砂纸将其表面打磨光亮.
②在金属活动顺序表中氢前边的金属可以与稀硫酸反应,但氢以后的金属不会与稀硫酸反应,所以铁会与稀硫酸反应,但银不会与稀硫酸反应,铁与稀硫酸反应时生成氢气和硫酸亚铁溶液:Fe+H
2SO
4=FeSO
4+H
2↑,因为Fe
2+显绿色,所以观察到的现象是铁丝表面有气泡产生,溶液由无色变为浅绿色,而银丝表面无明显现象.
③金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以在金属活动顺序表中在铁和银之间找一种金属的盐溶液,如硫酸铜溶液,把铁和银两种金属插入该盐的溶液中,铁可以把该金属从其盐溶液中置换出来,但银不会把该金属从其盐溶液中置换出来.
(2)钛合金可以用来制人造骨、制造船舶、制造航天飞机.故填:②③④.
(3)金属越活泼的越不容易制取,所以与金属活动性有关.故选③;
(4)由题中信息在高温条件下用H
2和FeCl
2发生置换反应,生成“纳米铁”.可知反应物为氢气和氯化亚铁,生成物为铁,根据反应前后元素种类不变可知另一生成物为氯化氢,化学方程式为FeCl
2+H
2
Fe+2HCl;铁在热的时候活动性很强,故应使用保护气防止铁在高温下与氧气反应.
故答案为:(1)①用砂纸将铁丝和银丝表面打磨光亮;②Fe+H
2SO
4=FeSO
4+H
2↑,比较铁和银的金属活动性强弱;③CuSO
4,Cu.
(2)②③④.(3)③;
(4)FeCl
2+H
2
Fe+2HCl,防止铁在高温下与氧气反应.
分析:(1)根据金属活动顺序表中铁、铜、银的金属活动性强弱去作答,这三种金属的金属活动性由强到弱的顺序为铁>铜>银;
(2)钛合金具有优良性能,具有广阔的发展前景.
(3)根据制取的难易程度考虑;
(4)根据反应物生成物进行书写解决,注意条件;铁在热的时候活动性很强,故应使用保护气
点评:会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

 金属是一类重要的材料,人类的生活和生产都离不开金属.
金属是一类重要的材料,人类的生活和生产都离不开金属. Fe+2HCl;铁在热的时候活动性很强,故应使用保护气防止铁在高温下与氧气反应.
Fe+2HCl;铁在热的时候活动性很强,故应使用保护气防止铁在高温下与氧气反应. Fe+2HCl,防止铁在高温下与氧气反应.
Fe+2HCl,防止铁在高温下与氧气反应.

 阅读快车系列答案
阅读快车系列答案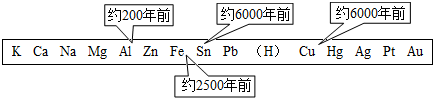


 金属是一类重要的材料,人类的生活和生产都离不开金属.
金属是一类重要的材料,人类的生活和生产都离不开金属.