
科目:初中化学 来源: 题型:
 右图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为紫红色固体单质.请回答下列问题:
右图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为紫红色固体单质.请回答下列问题:
查看答案和解析>>
科目:初中化学 来源: 题型:

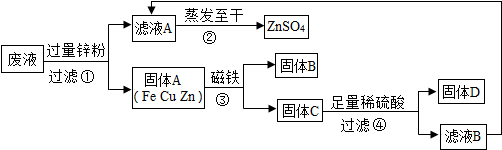
查看答案和解析>>
科目:初中化学 来源: 题型:
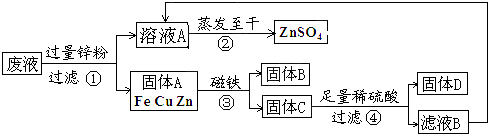
查看答案和解析>>
科目:初中化学 来源:课课练 初三化学 三年级全一册·配人教版 题型:013
某FeSO4和Fe2(SO4)3组成的混合物,经测定其中氧元素的质量分数为44%,则此混合物中Fe元素的质量分数为
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com