
| 二氧化锰与氯酸钾的质量比 | $\frac{1}{40}$ | $\frac{1}{20}$ | $\frac{1}{10}$ | $\frac{1}{5}$ | $\frac{1}{3}$ | $\frac{1}{2}$ | $\frac{2}{3}$ | $\frac{1}{1}$ | $\frac{2}{1}$ |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
分析 (1)根据反应原理以及化学方程式的写法来分析;
(2)根据反应的产物以及反应条件来分析;
(3)生成1L氧气的时间越短,速率就越快;从图表观察可以发现:二氧化锰最多时(2:1)时,生成1L二氧化碳所需时间相反最长(240).
解答 解:(1)过氧化氢在二氧化锰的催化作用下分解为水和氧气;氯酸钾在二氧化锰的催化作用下加热分解为氯化钾和氧气;高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)用双氧水制取O2更生成物只有水和氧气,且无需加热,节能环保;故填:节能、环保;
(3)观察图表不难发现,生成1L氧气的时间越短,速率就越快,从图表中看出,1:10时生成1L二氧化碳时间最短,在这一比值的前、后反应速率变化规律分别是增大、减小;在这一比值前所呈现的反应速率变化规律的原因是二氧化锰与反应物的接触面增大.故答案为:1:10;增大;减小;二氧化锰与反应物的接触面增大.
点评 本题考查了用实验室制取氧气,探究了催化剂二氧化锰的用量及作用,要充分利用题目给出的信息进行解答.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象及结论 |
| 取少量黄色粉末放入试管中,加入适量水,然后将湿润的红色石蕊试纸伸入试管内,观察现象 | 若试纸变蓝,则黄色固体是Mg3N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
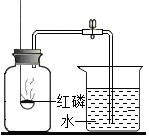 为测定空气里氧气的含量,甲、乙、丙三个小同学用如图所示的装置分别进行了实验探究.
为测定空气里氧气的含量,甲、乙、丙三个小同学用如图所示的装置分别进行了实验探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
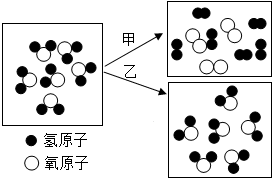 化学与生活息息相关.
化学与生活息息相关.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于氧化物 | |
| B. | 每个分子中含有8个原子 | |
| C. | 二甲醚有2个碳原子6个氢原子和一个氧原子组成 | |
| D. | 它是由碳、氢、氧三种元素组成的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com