

| A. | 元素A、B、C分别表示碳、氢、氧 | |
| B. | 该物质化学式可表示为CH6O2 | |
| C. | 该物质相对分子质量为105 | |
| D. | 分子中碳、氢、氧三种原子个数比为2:6:1 |
分析 由该物质的分子结构模型图,1个分子由2个C原子、6个A原子和1个B原子构成,则其化学式为:C2A6B.
A、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
B、由该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,据此进行分析判断.
C、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
D、由该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,据此进行分析判断.
解答 解:某物质由碳、氢、氧三种元素组成,由该物质的分子结构模型图,1个分子由2个C原子、6个A原子和1个B原子构成,则其化学式为:C2A6B.1个分子中含有6个氢原子,但A元素占13.0%,则A元素的原子相对原子质量较小,为氢元素;同理,则C元素为碳元素,B元素为氧元素.即其化学式为C2H6O.
A、该物质中碳、氢、氧元素的质量比为(12×2):(1×6):(16×1)=12:3:8,三种元素的质量分数由大到小的顺序分别是碳、氧、氢,则元素A、B、C分别表示氢、氧、碳,故选项说法错误.
B、由该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,则其化学式为:C2H6O,故选项说法错误.
C、该物质相对分子质量为12×2+1×5+16=46,故选项说法错误.
D、该物质的分子结构模型图,1个分子由2个碳原子、6个氢原子和1个氧原子构成,分子中碳、氢、氧三种原子个数比为2:6:1,故选项说法正确.
故选:D.
点评 本题有一定难度,由该物质的元素质量分数圆饼图、该物质的分子结构模型图确定该物质的化学式是正确解答本题的关键.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案科目:初中化学 来源: 题型:填空题
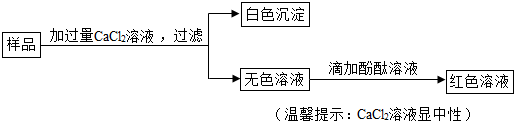
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
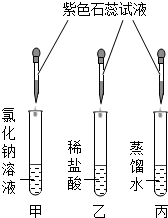 科学实验方案是根据特定实验目的而设计的.学习了“酸能使紫色石蕊试液变色”的知识后,进一步了解到“盐酸能电离产生H+和Cl-,氯化钠能电离产生Na+和Cl-”.为深入研究某一问题,小科同学设计了如图所示的实验方案,请回答:
科学实验方案是根据特定实验目的而设计的.学习了“酸能使紫色石蕊试液变色”的知识后,进一步了解到“盐酸能电离产生H+和Cl-,氯化钠能电离产生Na+和Cl-”.为深入研究某一问题,小科同学设计了如图所示的实验方案,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
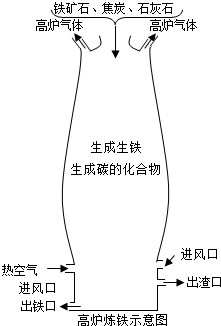 (1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.
(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )| 选项 | 甲物质 | 乙物质 | y轴表示的含义 |
| A | 二氧化锰 | 过氧化氢溶液 | 二氧化猛的质量 |
| B | t℃的水 | 硝酸钾 | t℃时硝酸钾的溶解度 |
| C | 氯化银 | 稀硝酸 | 氯化银的质量 |
| D | 饱和石灰水 | 生石灰 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
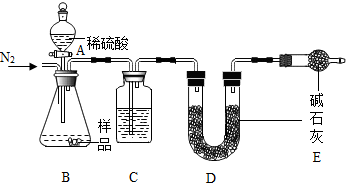 已知NaHCO3在270℃时完全分解为碳酸钠、水和二氧化碳.而Na2CO3受热不分解.现有某工厂生产出的一批
已知NaHCO3在270℃时完全分解为碳酸钠、水和二氧化碳.而Na2CO3受热不分解.现有某工厂生产出的一批查看答案和解析>>
科目:初中化学 来源: 题型:选择题
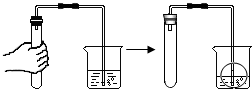 如图所示,龙龙同学采用手握试管外壁的方法检查装置的气密性,若装置的气密性良好,则将双手移开一会后,烧杯内导管处的现象(画圈部分)是( )
如图所示,龙龙同学采用手握试管外壁的方法检查装置的气密性,若装置的气密性良好,则将双手移开一会后,烧杯内导管处的现象(画圈部分)是( )| 选项 | A | B | C | D |
| 现象放大图 |  | 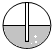 | 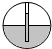 | 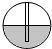 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应为化合反应 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 该反应中,乙、丁的质量变化之比为7:5 | |
| D. | 该反应中,甲、乙的质量变化之比为1:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com