
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
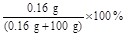 ②C
②C 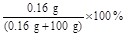 ;
;

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源:不详 题型:单选题

| A.操作步骤应为①②③④⑤ |
| B.操作③中得到的晶体可能是纯净物 |
| C.操作⑤后溶液的溶质只有一种 |
| D.最后剩余的溶液一定是两者的饱和溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题

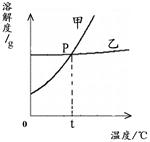
| A.硝酸钾的溶解度随温度升高而增大 |
| B.t1℃时,氯化钠和硝酸钾的溶解度相同 |
| C.要从含有少量氯化钠的硝酸钾溶液中得到较多的硝酸钾晶体,通常可采用降温结晶的方法 |
| D.t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com