


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| 序号 | 金属 | 熔点/℃ | 导电性 | 硬度 | 化学性质 | 金属冶炼的大致年限 |
| ① | Al | 660 | 61 | 2~2.9 | 常温下与氧气反应,表面形成致密的薄膜 | 约200年前 |
| ② | Fe | 1535 | 17 | 4~5 | 在潮湿的空气着火易生锈 | 约3000年前 |
| ③ | Cu | 1083 | 99 | 2.5~3 | 在高温时易与氧气反应 | 约6000年前 |
| ④ | Al | 660 | 61 | 2~2.9 | 常温下与氧气反应,表面形成致密的薄膜 | 约200年前 |

查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | 金属 | 熔点/℃ | 导电性 | 硬度 | 化学性质 | 金属冶炼的大致年限 |
| ① | Al | 660 | 61 | 2~2.9 | 常温下与氧气反应,表面形成致密的薄膜 | 约200年前 |
| ② | Fe | 1535 | 17 | 4~5 | 在潮湿的空气着火易生锈 | 约3000年前 |
| ③ | Cu | 1083 | 99 | 2.5~3 | 在高温时易与氧气反应 | 约6000年前 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
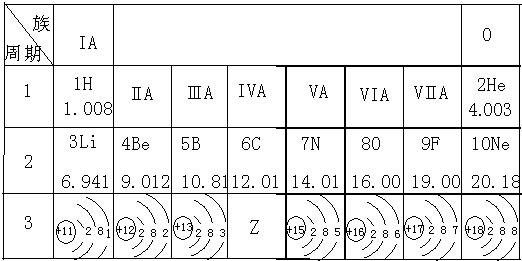
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | 1H 1.008 |
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He 4.003 |
| 2 | 3Li 6.941 |
4Be 9.012 |
5B 10.81 |
6C 12.01 |
7N 14.01 |
8O 16.00 |
9F 19.00 |
10Ne 20.18 |
| 3 |  |
 |
 |
Z |  |
 |
 |
 |


查看答案和解析>>
科目:初中化学 来源: 题型:
| 金属 | 熔点/℃ | 导电性 | 硬度 | 化学性质 | 冶炼的大致年限 |
| Al | 660 | 61 | 2~2.9 | 常温下与氧气反应,表面形成致密的薄膜 | 约200年前 |
| Fe | 1535 | 17 | 4~5 | 在潮湿的空气中易生锈 | 约3000年前 |
| Cu | 1083 | 99 | 2.5~3 | 在高温时与氧气反应 | 约6000年前 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com