
【题目】化学促进科学技术发展
(1)新高能材料的研究
2017年1月27日,《科学》上报道我国科学家团队成功合成世界首个全氮阴离子盐,占领新一代超高能含能材料研究国际制高点。该盐可简略表示如左图,请仔细观察下图:
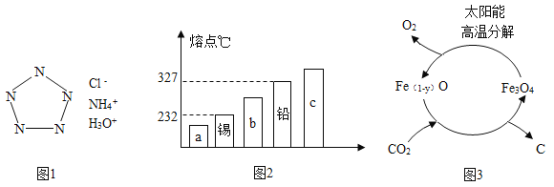
①由5个氮原子构成的全氮阴离子的符号是________。
②全氮阴离子盐化学式可表示为__________________。
(2)合金材料的研发
①合金的很多性能与组成它们的纯金属不同.图1能表示锡铅合金的是_____(填序号“a”“b”或“c”)。
②镁合金被誉为“21世纪绿色金属结构材料”。Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是___________(任写一个化学方程式)。该合金是一种储氢材料,完全吸氢后得到MgH2和Al,“储氢过程”属于________(填“物理”或“化学”)变化。
(3)CO2的绿色利用
①目前处理CO2的一种方法是在催化剂作用下,利用H2使CO2转化为甲烷并得到水。该反应的化学方程式为_____________。
②如图2是以“铁氧化物”为催化剂,利用太阳能将CO2资源化利用的方法之一,这一转化过程中总的化学方程式可表示为______________。
【答案】N5- NH4N5HCl a 4Al+3O2![]() 2Al2O3或2Mg+O2
2Al2O3或2Mg+O2![]() 2MgO 化学 4H2+CO2
2MgO 化学 4H2+CO2 CH4+2H2O CO2
CH4+2H2O CO2 C+O2
C+O2
【解析】
(1)由图可知,全氮阴离子是由5个氮原子包围一个负电荷,故填写:N5-;
由图可知,全氮阴离子盐包含有N5-、NH4+、H+、Cl-,化学式为:NH4N5HCl,故填写:NH4N5HCl;
(2)根据合金的的硬度比组成它的纯金属大,熔点比其纯金属小的原则可知,锡铅合金的熔点比锡、铅小,故填写:a;
Mg17Al12需在真空中熔炼的原因是,金属镁和铝在熔炼过程中易与空气中的氧气反应,使生成Mg17Al12的原料减少,故填写:4Al+3O2![]() 2Al2O3或2Mg+O2
2Al2O3或2Mg+O2![]() 2MgO;
2MgO;
Mg17Al12完全吸氢后得到MgH2和Al,物质发生了变化,属于化学反应,故填写:化学;
(3)H2在催化剂作用下使CO2转化为甲烷并得到水,化学方程式为:4H2+CO2 CH4+2H2O;故填写:4H2+CO2
CH4+2H2O;故填写:4H2+CO2 CH4+2H2O;
CH4+2H2O;
由图2可知,Fe3O4和Fe(1-x)O,在两个反应后,是循环的,质量不变,总反应中不出现,总反应中的反应物为二氧化碳,生成物为碳和氧气,故填写:CO2 C+O2。
C+O2。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】已知A-F六种物质均为初中化学常见物质,其中B、D为氧化物,A、B、E、F为不同类别的化合物,A、B、E放入水中能使酚酞变红,右下图是它们之间的关系 (部分反应物和产物已省略;“→”表示转化,“-”表示相互反应)。 请回答:
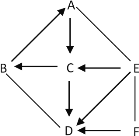
(1)写出B的化学式_________;固态物质A的俗名_____________。
(2)写出下列反应的化学方程式:
E→C__________________________________;
C→D__________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量。下列说法正确的是
A.K2Cr2O7中铬元素的化合价为+7B.K2Cr2O7属于氧化物
C.C2H5OH的相对分子质量为46D.C2H5OH中C、H、O的原子个数比为2:5:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具。下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题:
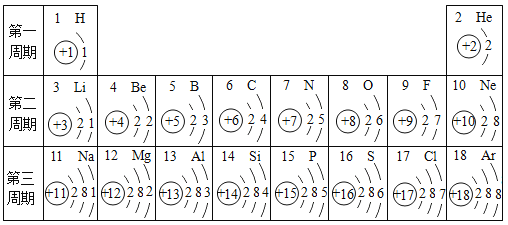
(1)硫元素的原子序数是___________,它属于_________(填“金属”成“非金属”)元素,表中氖元素位于元素周期表中的第_______周期。
(2)与元素的化学性质关系最密切的是原子的________;决定元素质量的是原子的________;硅元素和氧元素不同原因是______________。
(3)第三周期核外电子排布的规律是___________。
(4)写出核外电子排布与氖原子相同的阳离子符号是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是
A. 叶酸的相对分子质量为441 g
B. 叶酸中氮元素的质量分数大于氧元素的质量分数
C. 叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D. 叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MnSO4H2O在工业、农业等方面有广泛的应用。
(一)制备:工业上用化工厂尾气中低浓度SO2与软锰矿(主要成分MnO2,杂质金属元素Mg、Al、Fe等)制备MnSO4H2O过程如下:
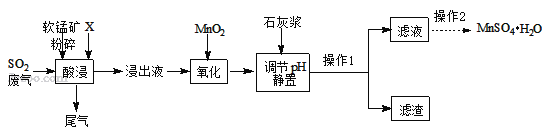
已知:浸出液中阳离子主要有H+、Mn2+、Mg2+、Fe2+、Al3+等;浸出过程中发生的主要反应化学方程式为:MnO2+SO2=MnSO4。
(1)生产中将软锰矿粉碎的目的是____。
(2)物质X最好选用_____。
a.盐酸 b.硫酸 c.硝酸
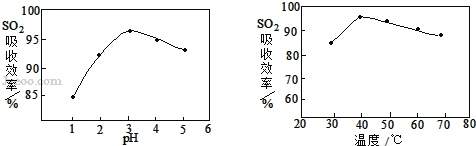
(3)酸浸时SO2的吸收效率与pH、温度的关系如下图所示,为提高SO2的吸收效率,酸浸时pH控制在____左右,温度控制在_________℃左右最适宜。
(4)流程中“氧化”步骤的目的是将Fe2+ 氧化为Fe3+,请完善反应的化学方程式MnO2+2FeSO4+_______ = MnSO4 + Fe2(SO4)3 + 2H2O 。
(5)加入石灰浆调节pH,可将氧化后的浸出液中杂质离子形成氢氧化物除去。
已知:(一)有关氢氧化物沉淀pH对应表
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Mg(OH)2 |
开始沉淀pH | 1.8 | 4.1 | 8.3 | 9.4 |
完全沉淀pH | 3.2 | 5.0 | 9.8 | 12.4 |
(二)Fe3+能与KSCN溶液作用显血红色则加石灰浆时应控制溶液的pH范围为_________。测定溶液的pH最好选____(a.pH试纸 b.pH计),检验Fe3+是否除尽的最佳方法是________。
(6)操作1包括过滤和洗涤,过滤用到的玻璃仪器有烧杯、玻璃棒和_____,洗涤的目的是________
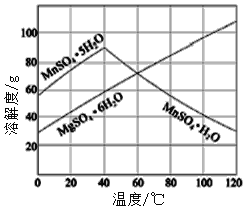
(7)已知硫酸锰、硫酸镁结晶水合物的溶解度曲线如图,则操作2包括:蒸发浓缩,___________,过滤、洗涤、干燥。
(二)应用:
(8)用MnSO4可测定水中溶解氧。方法是:取100mL 水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用0.79gL﹣1Na2S2O3溶液和I2反应,当消耗Na2S2O3溶液 12.0mL时反应完全。有关化学反应方程式下:
①2MnSO4+O2+4NaOH=2MnO(OH)2+2Na2SO4;
②MnO(OH)2 + 2KI + 2H2SO4 = MnSO4 + K2SO4 + I2 + 3H2O;
③I2 + 2Na2S2O3 = Na2S4O6 + 2NaI。
计算水样中溶解氧的浓度(以mgL-1为单位),写出计算过程________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组选择燃烧镁带进行定量实验研究
(资料)镁除了与空气中的氧气反应外,还可以与空气中的氮气在点燃条件下生成固体氮化镁Mg3N2,第一组同学称量了0.2g镁带,在空气中点燃,完全燃烧后,称量所得固体质量为0.30g。第二小组同学觉得第一小组的实验数据不合理,分析原因并设计了如下图所示的实验,实验步骤如下:
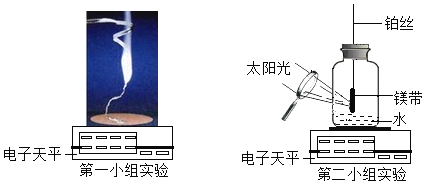
步骤一:将0.24g打磨光亮的镁带固定在穿过瓶塞的铂丝上(铂丝不反应),广口瓶盛满氧气并塞紧瓶塞(如图所示),瓶底留有适量的水;
步骤二:有聚光镜引燃镁带,待其完全燃烧后,充分震荡瓶内的水再静置,瓶内白烟完全消失,有白色固体沉淀在瓶底;(此条件下氧化镁难溶于水且不与水反应)
步骤三:将瓶内全部的固液混合物过滤,干燥滤纸及其表面的滤渣后一起称量,总质量为0.75g.(固体损失忽略不计)
请回答下列问题:
(1)写出镁带在空气中燃烧的化学方程式(只写一个)_______
(2)关于两个小组实验的说法正确的是_____
A 第一组实验数据不合理是因为0.3g>0.24g,不遵守质量定律
B 第二组实验中的水既可以加速装置冷却,又可以通过水帮助收集瓶内的生成物
C 镁带燃烧时有白烟飘散的现象说明分子是永不停歇的作无规则运动的
D 通过第一组实验数据可以推测,镁在空气中燃烧一定生成了氮化镁
E 第二小组同学只需称量镁带燃烧前后封闭的广口瓶体系的总质量,即可验证质量守恒定律定律
(3)第二小组同学在进行实验时,若未打磨去除镁带表面的氧化膜,最后他们称量的滤纸和滤渣总质量会____0.75g(填> < =)
(4)根据第二小组同学的实验数据,若要得到与氧气反应的质量,还必须测量___若实验结果与质量守恒向吻合,请推测以上测量值为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图回答简题
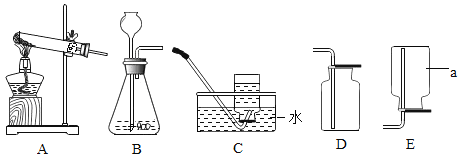
(1)写出仪器a的名称:______________。
(2)实验室用加热高锰酸钾的方法制取并收集氧气,应选用的发生装置为___________(填序号,下同),若要收集较纯净的氧气,则收集装置为______________。
(3)实验室用过氧化氢溶液和二氧化锰制取并收集氧气,若用D收集,则检验氧气是否收集满的操作为______________,制取氧气反应的文字表达式为______________。
(4)比较上述两种制取氧气的方法,请指出用过氧化氢溶液和二氧化锰制取氧气的优点有(写一条即可)_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电影《流浪地球》开创了中国科幻电影的新里程。描写了太阳在因老化形成“氮闪”而将毁灭地球的情况下,人类是如何应对一系列生存危机的。
(1)画出氦原子的结构示意图____________。
(2)当地球即将撞向木星时,木星表面的氢气与地球表面的大气混合,救援人员利用点燃混合气体时产生的巨大冲击力将地球推离木星,写出此反应的化学方程式_______________。该反应属于_____________(基本反应类型)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com