
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
(3)根据溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%,进行分析解答.
(4)要使溶液的溶质质量分数变大,常通过两种方式:①加入溶质,②蒸发溶剂,据此结合溶质质量分数的计算进行分析解答.
(5)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)40克质量分数为20的硝酸钠溶液,含溶质的质量为40g×20%=8g,溶剂的质量为40g-8g=32g.
(2)溶液稀释前后溶质的质量不变,若向上述溶液加入20克水,则所得溶液中溶质质量分数为$\frac{8g}{40g+20g}$×100%≈13.3%.
(3)若向上述溶液中加入10克硝酸钠,则所得溶液中溶质质量分数为$\frac{8g+10g}{40g+10g}$×100%=36%.
(4)设需要再溶解该物质的质量为x,(40g+x)×25%=40g×20%+x,x≈2.7g.
设需要蒸发水的质量为y,(40g-y)×20%=40g×10%,y=20g.
(5)若使上述溶液中溶质质量分数变为10%,设应加入水的质量为z,(40g+z)×10%=40g×20%,z=40g.
故答案为:(1)8g;32g;(2)13.3%;(3)36%;(4)2.7;20g;(5)40.
点评 本题难度不大,掌握溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶液稀释前后溶质的质量不变、溶质质量=溶液质量×溶质的质量分数等是正确解答此类题的关键所在.


 优学名师名题系列答案
优学名师名题系列答案科目:初中化学 来源: 题型:选择题
| A. | X>Y>Z | B. | Y>X>Z | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | pH越小,溶液的酸性越强 | |
| B. | 所有作物都适宜在PH在6.5--7.5的土壤中生长 | |
| C. | 稀盐酸遇到紫色石蕊试液变红 | |
| D. | 胃酸过多的病人在空腹时最好多喝些柠檬汁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
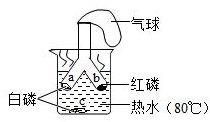 为探究燃烧所需的条件,某兴趣小组同学设计了如下图所示的装置.
为探究燃烧所需的条件,某兴趣小组同学设计了如下图所示的装置.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:【全国市级联考】重庆市2017届九年级中考仿真模拟化学试卷 题型:简答题
某兴趣小组对部分变质的氢氧化钠固体进行提纯,设计了如下操作流程:请回答:
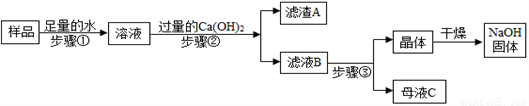
(1)步骤②反应的化学方程式为_______________________;加入过量Ca(OH)2的目的是_____________________________.
(2)滤液B中的溶质是_____________ 、_____________(写化学式);步骤③所包含的具体操作是加热浓缩、________________ 、过滤.
查看答案和解析>>
科目:初中化学 来源:【全国市级联考】重庆市2017届九年级中考仿真模拟化学试卷 题型:选择填充题
下列物质的鉴别、除杂的试验中所用的试剂或方法正确的是( )
选项 | 实验目的 | 所用试剂或方法 |
A | 鉴别CO和CO2 | 闻气味 |
B | 鉴别稀硫酸和稀盐酸 | 加氯化钡溶液 |
C | 除去生石灰中杂质石灰石 | 加水 |
D | 除去氧化铜中碳粉 | 加稀硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源:广东省东莞市堂星晨学校2017届考考前模拟(一)化学试卷 题型:探究题
材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料.
这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是____________________.
(2)钢铁材料通常分为生铁和钢.如图1是我国1997年发行的纪念钢产量首次突破1亿吨的邮票.邮票通常密封保存在聚乙烯塑料袋中
①以上叙述中不涉及到的材料是_________________(选填序号).
A.合金 B.无机非金属材料 C.有机合成材料
②以赤铁矿为原料冶炼铁反应的化学方程式 _________________________________________。
③钢铁露置在空气中易生锈,请提出防止其生锈的一种措施____________________.
(二)铁及其化合物的实验
(3)将Fe粉溶于稀H2SO4,此反应属于_____(填基本反应类型).用点燃法检验生成的H2前必须______.
(4)向上述反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色.
①生成Fe(OH)2反应的化学方程式_______________________________.
②白色沉淀变为灰绿色的原因之一是部分Fe(OH)2接触空气生成Fe(OH)3,反应的化学方程式_____________.生成的Fe(OH)3分解为Fe2O3.
③过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO4•2Fe(OH)2•Fe2O3〔相对分子质量为644].能证明固体已洗净的方法为__________________________________.
(三)灰绿色固体的热分解实验
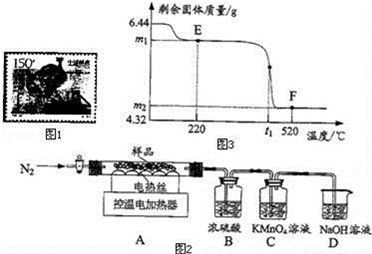
兴趣小组称取此固体6.44g,在科研人员的指导下用如图2装置进行热分解实验.
[查阅资料]
①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3,2FeSO4 Fe2O3+SO2↑+SO3↑.
Fe2O3+SO2↑+SO3↑.
(5)加热前后及过程中均通入N2,加热前通N2的目的是_____________________________.
(6)控制温度在不同的范围对A中样品加热,测得剩余固体质量随温度的变化如图3所示.B装置中浓硫酸只能吸收SO3和H2O,当加热到t1℃时,装置C中的现象为______________.
①图3中E点对应的m1= ______________.
②图3中F点对应物质中Fe2O3的质量为__g.
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe3O4.已知加热过程中发生两个反应,且反应前后固体总质量不变.请写出其中一个反应的化学方程式______________________.
查看答案和解析>>
科目:初中化学 来源:【全国区级联考】南京市六合区2017届九年级中考二模化学试卷 题型:信息分析题
人类社会的发展离不开金属。
(1)“沙里淘金”说明金在自然界中有_________(填“单质”或“化合物”)形式存在。
(2)下列不属于合金的是______(填序号)。
A.氧化铁 B.不锈钢 C.铝 D.焊锡
(3)金属矿物的储量有限,而且不能再生。保护金属资源的有效途径除防止金属的腐蚀外,还有________________________等(写出一条即可)。
(4)将铁丝浸入硫酸铜溶液中,发生反应的化学方程式是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com