小明同学打算自己探究一下MnO2在分解过氧化氢时所起的作用,但手边没有现成的MnO2药品,只有高锰酸钾,30%过氧化氢溶液、木条、水、火柴,其它仪器可任选.
(1)若要先得到MnO2粉末,反应原理是(用化学式表示化学反应)________,装置为________(用图示)
(2)已知实验(1)中试管中剩下两种物质,其中二氧化锰难溶于水,而另一种易溶于水,小明用了一种方法将它们分离开来,步骤为:①________,②________.
(3)小明认为若要探究MnO2在较低的温度下对分解H2O2有无催化作用,需作对比实验,他设计了三组实验:
①在试管中加入5ml 30%的过氧化氢溶液,把带火星的木条伸入试管,看木条是否复燃.
②…;
③在第3支试管中加入5ml 30%过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃.
你认为小明设计的第2组实验过程应为:________.
(4)小明得到的是③中有O2放出,但他认为③中有O2放出是因为MnO2与H2O2发生了反应,你如何帮他设计实验来说明MnO2没有和H2O2起反应,而只是起了催化作用?
解:高锰酸钾加热生成锰酸钾、二氧化锰和氧气.生成的二氧化锰可做催化剂.利用锰酸钾和二氧化锰在水中的水溶性不同,可将二氧化锰分离开来.在验证二氧化锰做催化剂时,首先设计只有双氧水时,是否能迅速放出氧气.再设计只有二氧化锰时,能否放出氧气.
故答案为:(1)KMnO4

K
2MnO
4+MnO
2+O
2;试管、铁架、酒精灯.
(2)溶解;过滤.
(3)在第二支试管加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃.
(4)将反应后所得固体过滤,洗涤,然后再将所得的固体加入盛双氧水的试管中,然后在试管口处,放一带火星的木条,观察木条复燃,说明二氧化锰没有跟双氧水发生反应,只是改变反应速率.
分析:催化剂是改变化学反应的速率,而反应前后催化剂的质量和化学性质保持不变.
点评:在验证二氧化锰的质量反应前后是否改变,可将反应后的固体过滤,干燥称量固体质量.

 K2MnO4+MnO2+O2;试管、铁架、酒精灯.
K2MnO4+MnO2+O2;试管、铁架、酒精灯.

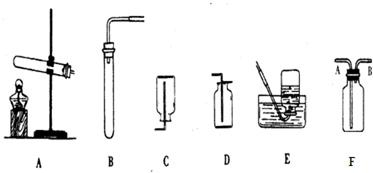 27、化学实验室里,老师给同学们准备了如下实验装置:
27、化学实验室里,老师给同学们准备了如下实验装置: