
科目:初中化学 来源: 题型:阅读理解
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | ||
| Ⅱ | 1.2g | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g |
 |
气体发生装置内物质的总质量 | |
| 反应前 | 35.6g | |
| 反应后 | 34.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
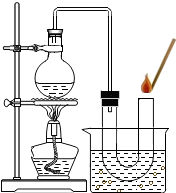 小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明将家中清洗伤口用的消毒液--“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.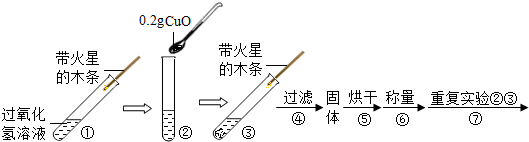
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中 有气泡冒出 有气泡冒出 ,带火星的木条复燃. |
仍为0.2g (或氧化铜质量不变) 仍为0.2g (或氧化铜质量不变) |
溶液中有气泡放出, 使带火星的木条复燃 使带火星的木条复燃 . |
猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立. |
| CuO |
| CuO |
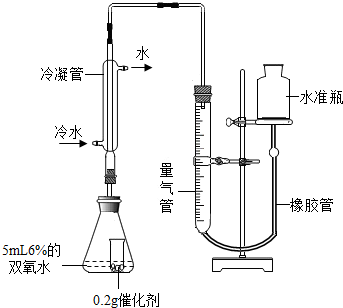 (9)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差
(9)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 1 |
| 5 |

| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
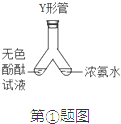
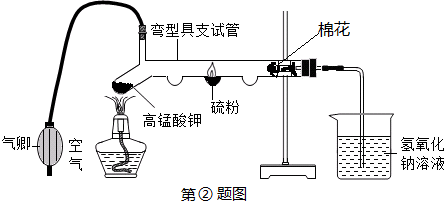
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com