
| 数据 | 实验1 | 实验2 | 实验3 | 实验4 | 实验5 |
| 加入稀盐酸的质量/g | 0 | 50 | 50 | 50 | 50 |
| 烧杯与烧杯中物质的总质量/g | 70.00 | 117.5 | 165.0 | M | 263.4 |
分析 (1)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,根据表中数据可知:实验4、实验5比较,实验4中M=263.4g-50=213.4g,
(2)根据质量守恒定律,反应前后的质量差即为反应生成二氧化碳的质量;
(3)根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算该鸡蛋壳中碳酸钙的质量分数.
解答 解:
(1)根据表中数据可知:实验4、实验5比较,实验4中M=263.4g-50=213.4g;
(2)根据质量守恒定律,生成二氧化碳的质量=70g+50g×4-263,4=6.6g
(3)故设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 6.6g
$\frac{100}{x}=\frac{44}{6.6g}$
x=15g
该鸡蛋壳中碳酸钙的质量分数=$\frac{15g}{20g}×$100%=75%.
答案:
(1)213.4;
(2)6.6g;
(3)该鸡蛋壳中碳酸钙的质量分数为75%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活中常用的塑料、纤维、合金等都是有机合成材料 | |
| B. | 缺锌会引起食欲不振,生长迟缓,发育不良.因此我们要大量补充葡萄糖酸锌 | |
| C. | 葡萄糖在人体内缓慢氧化,同时放出能量 | |
| D. | 脂肪、糖类、动物蛋白都是人体必须的营养素,吃得越多越好 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -1 | B. | +3 | C. | +5 | D. | +7 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
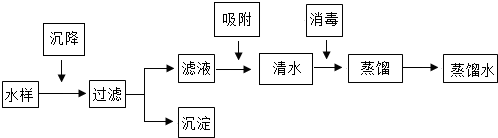
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
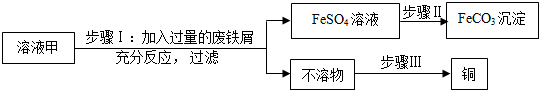
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
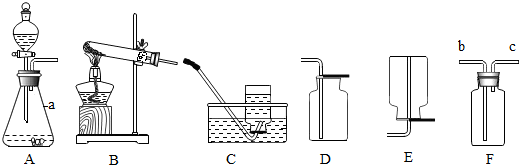
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
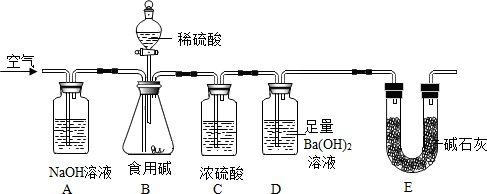
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com