
((7分)某纯碱样品中混有少量的氯化钠,为了测定该样品中碳酸钠的质量分数,小明同学准确称取 12.0g样品,做了如下实验: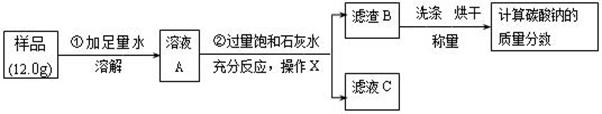
请回答下列问题:
(1)操作X用到的玻璃仪器除烧杯、玻璃棒外,还必需有 。
(2)滤液 C中的溶质是 ,若向滤液 C中滴加稀盐酸,写出过程中发生的一个中和反应的化学方程式 。
(3)若将滤渣B洗涤烘干后,称量其质量为 10.0g , 计算纯碱样品中的 Na2CO3的质量分数是多少?(结果保留一位小数,要求写出计算过程)
(1)漏斗(或普通漏斗)(2)氯化钠、氢氧化钠、氢氧化钙(写化学式也可,少答得1分、错答不给分);NaOH + HCl ="=" NaCl + H2O【或Ca(OH)2 + 2HCl ="=" CaCl2 +2H2O】
(3)88.3%
解析试题分析:(1)操作X是物质分为滤渣B和滤液C,所以操作应为过滤;用到的玻璃仪器除烧杯、玻璃棒外,还必需有漏斗。
(2)碳酸钠和氢氧化钙(石灰水的溶质)反应生成碳酸钙沉淀和氢氧化钠;所以滤液 C中的溶质有氢氧化钠;石灰水过量,则滤液C中还含有未反应的氢氧化钙;原样品中的氯化钠未发生反应,可进入滤液C中。所以滤液C中的成分为氢氧化钠、氢氧化钙和氯化钠。
若向滤液 C中滴加稀盐酸,则反应有:NaOH + HCl ="=" NaCl + H2O和Ca(OH)2 + 2HCl ="=" CaCl2 +2H2O。
(3)根据题意可知,已知量为滤渣B(碳酸钙)质量为 10.0g;未知量为样品中的 Na2CO3的质量分数。
解题思路:可根据碳酸钙和碳酸钠在反应中的质量关系,求出碳酸钠的质量,再进一步求出其质量分数。具体过程如下:
解:设要生成10.0g碳酸钙需要碳酸钠的质量为x
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
106 100
x 10.0g
106 : 100 =" x" :10.0g
X=10.6g
样品中碳酸钠的质量分数为: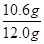 ×100% =" 88.3%"
×100% =" 88.3%"
答:样品中碳酸钠的质量分数为88.3%
考点:除杂、综合计算


科目:初中化学 来源: 题型:计算题
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6 分)镁是一种用途广泛的金属材料,目前大部分镁都是利用从海水中提取的镁盐 制取的。某校化学活动小组欲测定海水中氯化镁的含量,取海水样品 200g,加入适量 氢氧化钠溶液,至恰好完全反应为止,称量所得沉淀物的质量为 0.58g。 请你根据上述资料,回答下列问题:
⑴金属镁的物理性质有: 。(答出一条即可)
⑵查阅资料可知,海水中镁元素的含量比较低,所以,从海水中提取 MgCl2 时, 经历了“MgCl2 → Mg(OH)2 → MgCl2”的转化过程,请分析这样做的目的是
⑶列式计算:上述 200g 海水样品中,所含 MgCl2 的质量是多少?
(提示:MgCl2 + 2NaOH = Mg(OH)2↓ + 2NaCl )
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定部分变质的烧碱中氢氧化钠的质量分数,称取样品5.3g,加入10%的氯化钡溶液,至沉淀不再产生,洗涤、烘干、称量后得到沉淀0.01mol。
① 写出氢氧化钠变质的化学方程式 。
② 求样品中氢氧化钠的质量分数。(根据化学方程式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室有一瓶硫酸废液,老师请小红同学设计方案测定该废液中硫酸的质量分数.小红同学先取一纯净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸砂去铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9g.请回答下列问题:
(1)反应中产生的气体的质量是 。
(2)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数).
(3)如果铁钉的铁锈未除净,对(2)计算结果的影响是 (选填“偏大”、“偏小”、“无影响”),原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质)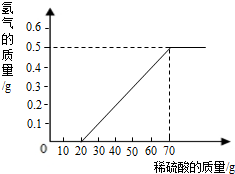
(1)当稀硫酸的质量为70g,产生的氢气的质量为0.5g
(2)用化学方程式说明当稀硫酸的质量为10g时,为什么不产生氢气 ;
(3)计算镁条中镁元素的质量分数(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数。
Ⅰ.甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化);反应生成单质铁和二氧化碳,以及少量的一氧化碳。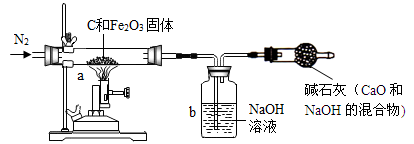
(1) 实验中持续通入干燥的氮气。加热前缓缓通入一段时间,其作用是 。
(2)反应结束后,甲同学熄灭了喷灯的火焰后,马上停止通入N2,他这样操作引起的后果
是 。
(3)如果b装置中氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用b装置中氢氧
化钠溶液的质量变化测定出氧化铁的质量分数将 (选填“偏大”、“偏小”
或“准确”)。
Ⅱ.乙同学取氧化铁的质量分数为80%的赤铁矿粉10g,加入足量稀盐酸,恰好完全反应,
共用去稀盐酸154.5g(假设杂质既不溶于水也不与酸发生反应)。
试计算反应后溶液中溶质的质量分数。(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)为测定某纯碱样品(含氢氧化钠杂质)中碳酸钠的含量,进行如下实验:取65g纯碱样品平均分为5份,分别加入相同质量分数的稀盐酸溶液,获得如下实验数据:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 样品质量/g | 13 | 13 | 13 | 13 | 13 |
| 加入盐酸质量/g | 15 | 30 | 80 | 130 | 150 |
| 反应后物质质量/g | 28 | 43 | 90.8 | 138.6 | 158.6 |
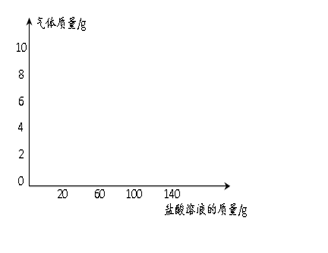
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将117.0g氯化钠溶液与140.0g的硝酸银溶液混合,恰好完全反应,过滤后所得溶液的质量为228.3g。计算该氯化钠溶液的溶质质量分数?
(反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com