
| 催化剂 温度/℃ 反应程度 | 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |


分析 【查阅资料】比较表格中开始反应的温度和剧烈反应的温度,可以发现氧化铜的两个温度都比较低,方便操作.
【设计并完成实验】根据已有的知识进行分析,进行实验探究时要注意控制变量;根据控制双氧水的质量和质量分数相等才能比较出二氧化锰和氧化铜的催化效果分析.
【讨论交流】(1)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(2)根据图中给出的比例分析.
解答 解:比较表格中开始反应的温度和剧烈反应的温度,可以发现氧化铜的两个温度都比较低.温度越低,加热反应时就越方便操作,所以氧化铜作催化剂最合适;
【设计并完成实验】
氯酸钾在二氧化锰的催化作用下加热能快速的产生氧气,进行实验探究时要注意控制变量,故X为3.0;Ⅰ与Ⅲ比较证明了氧化铜也可以加快氯酸钾的分解速率;根据催化剂的定义可以知道,要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的质量和化学性质都没有改变;实验Ⅲ中的化学反应为:2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑;Ⅱ与Ⅲ对比的目的是比较氧化铜与二氧化锰哪种物质对氯酸钾的催化作用更好;
【讨论交流】
(1)根据图示可以看出H2O2的用量越多,产生的氧气越多;
(2)由图示可知3%H2O2溶液8毫升与0.08克MnO2混合,分解速度达到实验要求,若MnO2的质量有4克需要3%H2O2溶液为$\frac{4g}{0.08g}$×8mL=400mL.
故答案为:
【查阅资料】氧化铜.
【实验现象分析】
3.0g,CuO改变KClO3分解的速率.
质量;化学性质.
【结论】2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑;
【实验反思】CuO对KClO3催化效果是否比MnO2好.
【讨论交流】
(1)过氧化氢的用量越多,产生的氧气越多.
(2)C.
点评 本题通过对比实验结果的分析,找到事物的内在联系,考查了学生分析问题的能力,同时也是对影响反应速率因素这一知识点的重点考查.


科目:初中化学 来源: 题型:填空题
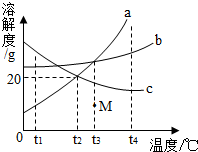 如图是a、b、c三种物质的溶解度曲线,请回答:
如图是a、b、c三种物质的溶解度曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
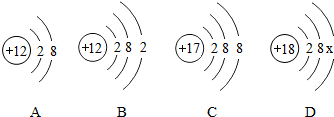
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③⑥ | C. | ③④⑤ | D. | ①④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3 | B. | Al(NO3)3 | C. | Fe(NO3)3 | D. | Fe2(SO4)3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +4 | B. | +3 | C. | -3 | D. | -1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com