

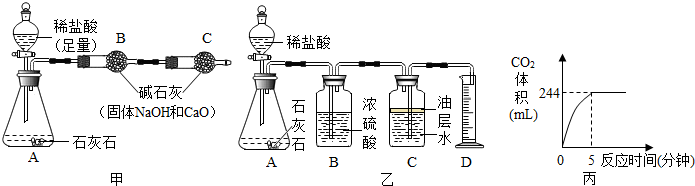
���� ��1�����������̼��Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼���ڶ��μ����ᣬ�����������٣�˵����һ����������ȫ��Ӧ��̼�����ʣ�࣬��֪50g������ȫ����5g̼��ƣ����ڶ��μ��ٵ�����Ϊ2.9g��˵��̼�����ȫ��Ӧ��ʣ����������������ʯ��ʯ��Ʒ�����ʵ��������н��
��2�����ݼ�ʯ��������ˮ�������Ȼ������壬B�����ն�����̼�д�����ˮ�������Ȼ���������н��
��3�����ݶ�����̼������ܶ����������̼�����������ö�����̼���������̼��Ƶ����������������ʯ��ʯ��Ʒ��CaCO3�������������ɣ�
��4������С���IJ����֪����Ӧ��5g̼�����Ҫ����50g��С���IJ����ǽ�20gϡ������뵽1.25g��Ʒ�У���ʱ20gϡ�����ǹ����ģ�����Ӧ����С���ɼ���ʵ�����ݼ��㣮
��� �⣺��1�������̼��Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼���ڶ��μ����ᣬ�����������٣�˵����һ����������ȫ��Ӧ��̼�����ʣ�࣬��֪50g������ȫ����5g̼��ƣ����ڶ��μ��ٵ�����Ϊ2.9g��˵��̼�����ȫ��Ӧ��ʣ����������������ʯ��ʯ��Ʒ�����ʵ���������Ʒ��̼��Ƶ���������Ϊ��$\frac{10g-2.1g}{10g}$��100%=79%��
��2����ʯ��������ˮ�������Ȼ������壬B�����ն�����̼�д�����ˮ�������Ȼ������壬�������̼��Ƶ�������������������ʵ���ز�����
��3��������̼������=1.8g/L��0.244L��0.44g����̼��Ƶ�����Ϊx
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 0.44g
$\frac{100}{x}$=$\frac{44}{0.44g}$
x=1g
��ʯ��ʯ��Ʒ��CaCO3����������Ϊ��$\frac{1g}{1.25g}$��100%=80%��
��4������С���ģ�����С���IJ����֪����Ӧ��5g̼�����Ҫ����50g��С���IJ����ǽ�20gϡ������뵽1.25g��Ʒ�У���ʱ20gϡ�����ǹ����ģ�����Ӧ����С���ɼ���ʵ�����ݼ��㣮
��֪��ȡ50g���ᣬ��Ӧ��̼�������Ϊ10g-5g=5g�����û�ѧ����ʽ��������Ȼ������������μӷ�Ӧ��ϡ�������������Ϊy��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 73 44
5g 50g��y
$\frac{100}{5g}$=$\frac{73}{50g��y}$
y=7.3%
�ʴ�Ϊ����1��79%��
��2��B�����ն�����̼�д�����ˮ�������Ȼ������壻
��3��80%��
��4������С���ģ�����С���IJ����֪����Ӧ��5g̼�����Ҫ����50g��С���IJ����ǽ�20gϡ������뵽1.25g��Ʒ�У���ʱ20gϡ�����ǹ����ģ�����Ӧ����С���ɼ���ʵ�����ݼ��㣮
7.3%��
���� ���⿼��ѧ�����û�ѧ��Ӧ����ʽ�ļ��㣬��ȷ������̼�����岢���������غ������������̼�������ǽ��Ĺؼ���


 ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д� ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
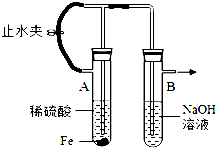 ��֪Fe��OH��2�ǰ�ɫ��״�����������ױ������е���������ΪFe��OH��3���ɫ��������ͼΪFe��OH��2�Ʊ�ʵ��ĸĽ�װ�ã�ʹ�ø�װ�����ڽϳ���ʱ���ڹ۲쵽���ɵ�Fe��OH��2��ɫ��״����������Ϊʵ����̣�
��֪Fe��OH��2�ǰ�ɫ��״�����������ױ������е���������ΪFe��OH��3���ɫ��������ͼΪFe��OH��2�Ʊ�ʵ��ĸĽ�װ�ã�ʹ�ø�װ�����ڽϳ���ʱ���ڹ۲쵽���ɵ�Fe��OH��2��ɫ��״����������Ϊʵ����̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������54��ԭ�ӹ��� | |
| B�� | ��������̼Ԫ������Ԫ�ص�������Ϊ9��17 | |
| C�� | �����ʵ���Է�������Ϊ282g | |
| D�� | ������������Ԫ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ȼ��ƺ�����ͭ�Ļ�������ܽ⡢���ˡ������ķ������� | |
| B�� | ������ƿ�зֱ�װ��O2��CO2��Ϊ�������ǣ��ɵ�������NaOH��Һ���� | |
| C�� | ��BaCl2��Һ��ȥNaOH��Һ�л��е�����Na2SO4���� | |
| D�� | ����ZnCl2��Cu��AgCl���Եó�Zn��Cu��Ag���ֽ����Ļ��˳�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com