学习了教材中O
2的制法后,某小组同学查找资料知道,加热5%的H
2O
2溶液,也能够制得O
2,其反应的化学方程式为:2H
2O
2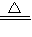
2H
2O+O
2↑
小组同学将5%的H
2O
2溶液放在试管中加热,用带火星的木条在试管口检验产生的O
2 时,发现带火星的木条很难复燃.
【猜想与假设】:
①产物中有水蒸气,带火星的木条不能复燃.
②产生的O
2量少,带火星的木条不能复燃.
【设计改进方案】:
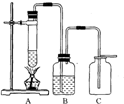
针对猜想①,甲同学设计了如右图所示的装置,B瓶中应盛放的干燥剂应是
.
针对猜想②,乙同学使用10%的H
2O
2溶液进行上述实验;丙同学向5%的H
2O
2溶液中加入2滴新制的NaOH溶液,加热一段时间.
三位同学用带火星的木条检验,均复燃.
【反思与评价】:
①甲同学设计的装置有一处不尽合理,请你做以下改进
.
②由乙同学的实验可得出,影响H
2O
2溶液产生O
2量的多少的因素可能是
.
③丙同学分析得出NaOH溶液所起的作用可能是
.
【拓展与交流】:
①资料表明:在常温下固体MnO
2与5%H
2O
2溶液混合同样能够制得O
2,你会选择与实验室制取
(填“O
2”或“CO
2”)相似的发生装置进行实验.
②与KMnO
4制取O
2比较,用5%H
2O
2溶液与MnO
2混合制得O
2有其优越性,如
,(答出-点即可).


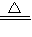 2H2O+O2↑
2H2O+O2↑


 学习了教材中O2的制法后,某小组同学查找资料知道,加热5%的H2O2溶液,也能够制得O2,其反应的化学方程式为:2H2O2
学习了教材中O2的制法后,某小组同学查找资料知道,加热5%的H2O2溶液,也能够制得O2,其反应的化学方程式为:2H2O2