
| A. | 过多CO2排放会导致“温室效应”,应提倡“低碳生活” | |
| B. | 一氧化碳易与血液中的血红蛋白结合,使人中毒 | |
| C. | 金刚石和石墨都是碳单质,但原子排列方式不同,物理性质也不同 | |
| D. | CO、CO2、大理石都属于化合物 |
分析 A、根据二氧化碳对环境的影响进行分析判断.
B、根据一氧化碳中毒的原理进行分析判断.
C、根据金刚石和石墨物理性质不同的原因,进行分析判断.
D、根据由不同种元素组成的纯净物是化合物,进行分析判断.
解答 解:A、过多CO2排放会导致“温室效应”,会造成全球气候变暖等,应提倡“低碳生活”,故选项说法正确.
B、一氧化碳易与血液中的血红蛋白结合,使人中毒,故选项说法正确.
C、金刚石和石墨都是碳单质,但原子排列方式不同,故物理性质不同,故选项说法正确.
D、CO、CO2都是由不同种元素组成的纯净物,均属于化合物;大理石的主要成分是碳酸钙,含有杂质,属于混合物;故选项说法错误.
故选:D.
点评 本题难度不大,了解二氧化碳对环境的影响、一氧化碳的毒性、常见的碳单质、化合物的特征等是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
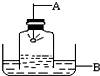 如图是空气中氧气含量的测定装置.回答下列问题:
如图是空气中氧气含量的测定装置.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
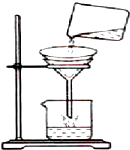 (1)如图是实验室过滤常用装置,但是其中有两处错误,请指出其中一处错误:没有玻璃杯引流(漏斗的下端没有紧靠接受的烧杯);
(1)如图是实验室过滤常用装置,但是其中有两处错误,请指出其中一处错误:没有玻璃杯引流(漏斗的下端没有紧靠接受的烧杯);查看答案和解析>>
科目:初中化学 来源: 题型:解答题
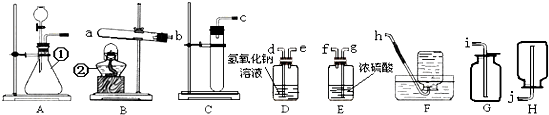
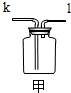
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com