
某化学实验小组为了除去混在N2中的O2,将混合气体通过红热的铜丝网后,发现铜丝网变黑。在研究如何除去黑色物质,回收再利用铜丝网的讨论中,制定了下列方案。
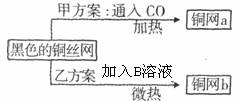
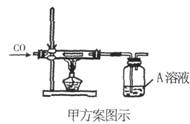
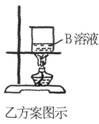
请根据以上方案回答:
(1)乙方案的烧杯中发生反应的化学方程式是(其中B物质自行确定)
。两种方案相比较,甲方案明显的不足之处是
。
(2)若采用甲乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量 (填“<”、“>”、“=”)铜丝网b的质量。
(3)实验小组的同学发现,反应后烧杯中的液体有腐蚀性,应加以适当的处理。他们采取加入铁粉的方案处理废液。加入足量的铁粉充分搅拌,最后得到的溶液中溶质为 。
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:初中化学 来源: 题型:
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 11 | 6 | 3.2 | n |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:
| 石灰石的用量 | 剩余固体的总质量 |
| 第一次加入5g | 1g |
| 第二次加入5g | 2g |
| 第三次加入5g | 3g |
| 第四次加入5g | 8g |
| 第五次加入5g | 13g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | 实验步骤 | 装置图 | 实验现象 | 解释或结论 |
(1) |
在盛有20℃水的烧杯中放入一小块白磷,并通入空气 |  |
无明显变化 |
温度没有达到白磷的着火点 温度没有达到白磷的着火点 |
(2) |
在盛有50℃水的烧杯中放入一小块白磷 |  |
无明显变化 无明显变化 |
白磷没有跟空气(或氧气)接触 |
(3) |
在盛有50℃水的烧杯中放入一小块白磷,并通入空气 |  |
白磷燃烧 |
白磷与空气接触且温度达到着火点 白磷与空气接触且温度达到着火点 |
(4) |
用坩埚钳夹取一小块大理石放在酒精灯火焰上加热 |  |
无明显变化 无明显变化 |
大理石不是可燃物 |
(5) |
在燃着的蜡烛火焰上方罩一个烧杯 |  |
蜡烛熄灭 | 蜡烛与空气隔绝 蜡烛与空气隔绝 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入10g | 3.0g |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.2g |
| 第四次加入10g | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com