
【题目】框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3·xH2O),E、F、I为无色气体。根据图示回答下列问题。
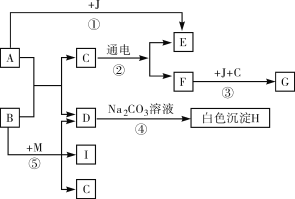
(1)写出有关物质的化学式:B_____,C_____。
(2)写出反应④的化学方程式_____。
(3)日常生活中为了阻止反应③发生,通常采取的措施是_____(写一条)。
(4)要使反应⑤能够发生,需要反应物B和M,其中M的化学式为_____。
【答案】Ca(OH)2 H2O CaCl2+Na2CO3=CaCO3↓+2NaCl 刷油漆、涂油等(其他合理答案均可) NH4Cl
【解析】
A是人体胃液中的一种成份,B可用于改良酸性土壤,G是铁锈的主要成份,因此A是盐酸,B是氢氧化钙,G是氧化铁;盐酸和氢氧化钙反应生成氯化钙和水,因此C是水,D是氯化钙;水通电分解得到氢气和氧气,盐酸和铁生成氯化亚铁和氢气,因此E是氢气,F是氧气,J是铁;氯化钙和碳酸钠反应生成碳酸钙白色沉淀和氯化钠,因此H是碳酸钙;由两种化合物互相交换成分生成另外两种化合物的反应叫复分解反应。氢氧化钙和氯化铵反应生成氯化钙和水和氨气,因此M是氯化铵,I是氨气,据此分析解答。
(1)由分析可知,有关物质的化学式为B:Ca(OH)2,C:H2O;
(2)反应④为氯化钙和碳酸钠反应生成碳酸钙白色沉淀和氯化钠,反应的化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl;
(3)铁生锈是铁与氧气和水蒸气共同作用的结果。日常生活中为了阻止反应③发生,通常采取的措施是:刷油漆、涂油等(其他合理答案均可);
(4)由分析可知,M是氯化铵,其化学式为:NH4Cl。


 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:
【题目】在化合物中,锑元素常显+3价或+5价。现有含锑元素的3种化合物:三氯化锑 SbCl3、三氧化二锑Sb2O3、锑酸钠NaSbO3。回答下列问题:
(1)用化学用语表示:
2个锑原子___________, SbCl3中含有的阳离子___________,锑酸钾__________。
(2)Sb2O5 是一种重要的阻燃剂。
①Sb2O5读作_________________;
②工业制取Sb2O5的化学方程式为:Sb2O3 + 2H2O2 =Sb2O5 + 2X,则X的化学式为_________。
(3)工业上常用碳与Sb2O3固体在高温下反应制得锑和二氧化碳,写出该反应的化学方程式是
_________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 温度升高时,物质的溶解度增大
B. 凡是均一、透明的液体就是溶液
C. 浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液
D. 20℃时36g氯化钠溶于100g水中,恰好达到饱和,此溶液中溶质的质量分数是36%
查看答案和解析>>
科目:初中化学 来源: 题型:
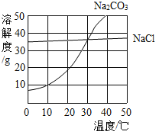
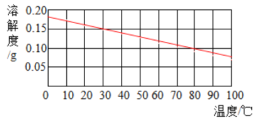
【题目】如图是氯化钠、碳酸钠和氢氧化钙的溶解度曲线
![]()
(1)碳酸钠和氯化钠的溶解度相等时对应的温度是__________。
(2)20℃时,分别向50g水中加入15g氯化钠和碳酸钠,充分溶解后形成饱和溶液的是______。
(3)将氢氧化钙的饱和溶液转化成不饱和溶液的方法是_______________________。
(4)碳酸钠中混有少量的氯化讷,可以用_____________的方法得到碳酸钠晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室里进行物质制备,下列各种利用原料及有关试剂制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是( )
A. C ![]() CO
CO![]() CO2
CO2 ![]() Na2CO3溶液
Na2CO3溶液
B. Cu ![]() Cu(NO3)2溶液
Cu(NO3)2溶液 ![]() Cu(OH)2
Cu(OH)2
C. Fe ![]() Fe2O3
Fe2O3 ![]() Fe2(SO4)3溶液
Fe2(SO4)3溶液
D. CaO ![]() Ca(OH)2溶液
Ca(OH)2溶液 ![]() NaOH溶液
NaOH溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学使世界变得绚丽多彩。
(1)2018年12月举世瞩目的港珠澳大桥正式通车。这个被誉为桥梁界“珠穆朗玛峰”的超级工程,桥梁主体首次大规模采用钢结构,它使用的42万吨钢铁足以建造60座埃菲尔铁塔、十座鸟巢,是迄今为止世界上最长的钢结构桥梁。

①大桥预计寿命120年,桥梁要求能抗16级台风、8级地震及30万吨巨轮撞击,撑起这座海上“钢铁巨龙”的不锈基座所用的是双相不锈钢钢筋。双相不锈钢钢筋属于_____(填序号)。
A合成材料 B复合材料 C金属材料
②大桥上的这些钢结构露置在潮湿的环境中极易发生锈蚀。设计师们在这些钢结构的外表面涂上了四氟型氟碳面漆树脂,为这座世纪大桥穿上了美丽的保护外衣。这种面漆防腐的原理是_____。
(2)大海是一个巨大的蓝色聚宝盆。大海中蕴藏着丰富的油气资源、煤和铁固体矿产、海底矿产资源、热液矿藏、可燃冰以及水产资源。中国在各海域油气储藏量约40~50亿吨。以南海为例,油气资源中可采部分约占66%,在西山群岛、中沙群岛的水下有上千米的新生代沉积物,是大有希望的海底石油和天然气产地;南海还蕴藏5万亿吨以上的锰、约3100亿吨镁、170亿吨锡和铜、29亿吨镍、8亿吨钴、5亿吨银、800万吨金、60亿吨铀等,比陆地矿产资源丰富得多;南海海洋鱼类有1500多种,如海龟、海参、龙虾、螺、贝等都具有极高经济价值的海产品。
①南海丰富的资源中,油气属于_____(填“纯净物”或“混合物”)。工业上对石油加热炼制时,根据各成分的_____不同可得到的产品有_____(写一种即可)。
②天然气燃烧的化学方程式是_____。
③文中所述“锰、镁、铜、……”等是指_____(填“元素”或“原子”)。
④海洋鱼类、海参、龙虾富含的营养素是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下,测得反应前后各物质的质量分数如图所示,下列说法正确的是_____。
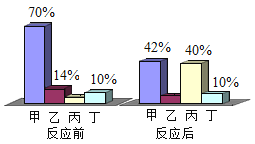
A. 丙可能是单质
B. 丁一定是该反应的催化剂
C. 该反应是化合反应
D. 该反应中乙、丙的质量比为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图1是以石灰石为原料制备高纯超细碳酸钙的工艺流程图:
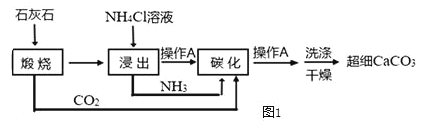
(1)流程中操作A的名称_____。实验室里该操作用到的玻璃仪器有烧杯、_____和_____。
(2)主要反应原理:
①“煅烧”步骤:主要反应的化学方程式为_____,反应基本类型为_____反应。
②“浸出”步骤:CaO+2NH4Cl=CaCl2+H2O+2NH3↑。
③“碳化”步骤:CO2+2NH3+H2O+CaCl2=CaCO3↓+2 NH4Cl。
(3)煅烧石灰石得到的固体中,除含CaO外,还含有少量MgO、FeO等杂质,在“浸出”过程为保证铁、镁等杂质不被浸出,需要适当提高溶液的pH.根据反应②计算出的钙铵比(参加反应的氧化钙和氯化铵的质量比)为_____,而实际流程中最佳钙铵比要稍高于这一比值,原因是_____。
(4)用上述流程可循环使用的物质除了H2O、CO2和NH3之外,还有_____。
(5)实验室在如图2装置中模拟上述流程制备高纯超细碳酸钙:
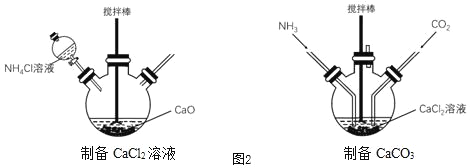
①搅拌的作用是_____。
②制备CaCl2溶液时需要对装置加热,主要作用是_____。
A 加快反应速率 B 促进氨气逸出
③已知在常温和一个标准大气压下,CO2和NH3在100g水中分别能溶解0.169g和52.9g。制备CaCO3时应先通入氨气后通入二氧化碳,理由是_____。
④浸取一步中NH4Cl溶液的溶质质量分数直接影响着生成CaCl2溶液溶质质量分数。已知0﹣100℃时NH4Cl的溶解度如下表:
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解(g) | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
如果用200g 80℃时NH4Cl的饱和溶液与纯氧化钙恰好完全反应,计算充分反应后得到CaCl2的质量_____。(写出计算过程,保留一位小数。)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】每年4、5月份是校园流感高发期,为此学校购买某品牌二氧化氯消毒液,如表为该消毒液的部分信息。
二氧化氯(ClO2)1000mL | |
溶质质量分数 | 80% |
密 度 | 1.2g/ml |
(1)二氧化氯(ClO2)中氯元素的化合价是_____。
(2)为预防流感,某校医务人员将其稀释至20%后,对全校教室进行全面消毒,从预防传染病的角度看,这属于_____(选“控制传染源”、“切断传播途径”或“保护易感人群”)。
(3)下列关于二氧化氯(ClO2)的说法正确的是_____。
A.二氧化氯由氯元素和氧元素组成
B.二氧化氯由二氧化氯分子构成
C.1个二氧化氯分子由1个氯原子和1个氧分子构成
D.二氧化氯中氯元素质量分数计算表达式为Cl%=![]() ×100%
×100%
(4)欲配制40kg质量分数为20%的稀二氧化氯消毒液,需要这种二氧化氯消毒液_____kg。
(5)当体内有炎症时会出现发热现象,这有利于吞噬细胞和杀菌物质等转移到炎症区,抵御病原体的攻击,此过程属于_____ (选“特异性免疫”或“非特异性免疫”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com