
 水是生命之源.
水是生命之源.分析 (1)根据硬水和软水与肥皂水混合的现象不同解答;
(2)电解水时根据“正氧负氢、氢二氧一”进行解答;
(3)根据溶质质量分数计算进行解答即可.
解答 解:
(1)硬水和软水与肥皂水混合的现象不同,可以使用肥皂水鉴别硬水和软水;
(2)电解水时正极产生的是氧气,负极产生的是氢气;
(3)配制500g溶质的质量分数为10%的葡萄糖溶液,需葡萄糖的质量为:500g×10%=50g,需要水的质量为500g-50g=450g;
故答案为:(1)肥皂水(2)氧气(3)50g 450g
点评 本题考查了水的净化的知识,完成此题,可以依据已有的知识进行.电解水实验图可知,与直流电源正极相连的玻璃管中生成的气体是氧气,负极产生的气体是氢气


科目:初中化学 来源: 题型:选择题
| A. | 用火碱溶液吸收二氧化硫SO2+2NaOH═Na2SO3+H2O | |
| B. | 植物的光合作用C6H12O6+6O2 $→_{光照}^{叶绿素}$6CO2+6H2O | |
| C. | 碳酸饮料中碳酸的形成原理CO2+H2O═H2CO3 | |
| D. | 利用一氧化碳的还原性得到金属铁2Fe2O3+3CO═4Fe+3CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
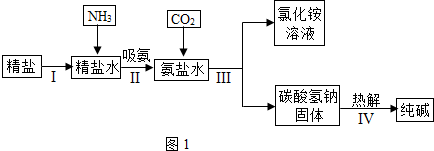
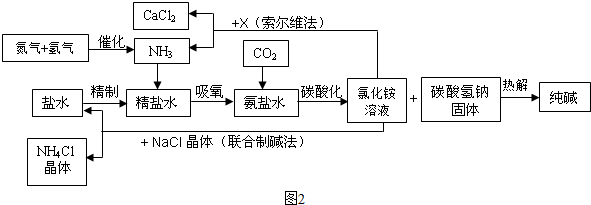
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质的应用 | 化学方程式 | 反应类型 |
| A | 电解水 | 2H202$\frac{\underline{\;通电\;}}{\;}$2H20+02↑ | 分解反应 |
| B | 向烧碱溶液中通人CO2 | 2NaOH+C02═Na2C03+H20 | 复分解反应 |
| C | 溶洞的形成 | CaC03+H20+C02═Ca(HC03)2 | 化合反应 |
| D | 比较铜和银的活动性 | Cu+AgN03═Cu(NO3)2+Ag | 置换反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HNO3、NaOH | B. | HCl、Na2CO3 | C. | NaCl、AgNO3 | D. | K2SO4、NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
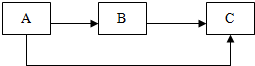 A、B、C均为初中化学常见物质,它们之间的转化关系如图所示(反应条件,部分反应物和生成物已略去).
A、B、C均为初中化学常见物质,它们之间的转化关系如图所示(反应条件,部分反应物和生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加过量BaCl2溶液 |
| 实验现象 | pH=10 | 产生白色沉淀 |
| 实验结论 | 溶液中有NaOH | 溶液中有H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com