“电石”是坚硬的块状固体,化学式为CaC
2.它有“服软不怕硬的脾气”,外力不易敲碎,但与水一接触就生成了氢氧化钙和乙炔(C
2H
2)气,本身却“消失”了.
①写出电石与水反应的化学方程式:
CaC2+2H2O═Ca(OH)2+C2H2↑
CaC2+2H2O═Ca(OH)2+C2H2↑
.
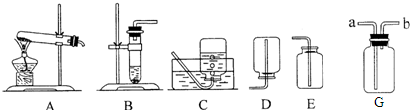
②标准状况下,乙炔气体的密度为1.161g/L(空气密度为1.293g/L),难溶于水.综上所述,若在实验室用“电石”制取乙炔,可用
B
B
装置(填字母编号,下同),收集较纯净的乙炔气时最好用
C
C
装置;如果用F装置收集乙炔气,气体从
b
b
管口进气(填“a或b”)
③乙炔在纯氧中燃烧时产生明亮的“氧炔焰”,生成二氧化碳和水,同时产生的高温可以熔化金属而达到焊接金属的目的.写出乙炔在氧气中完全燃烧的化学方程式:
④某同学用A、C装置制取并收集一瓶氧气,试管中所放化学药品的化学式是
KClO3和MnO2
KClO3和MnO2
,采用排水集气法收集氧气的原因是
氧气不易溶于水
氧气不易溶于水
.反应的化学方程式为
⑤若采用B和E装置制取氧气时,组装仪器时连接玻璃管和橡皮管的方法是先把玻璃管口
用水湿润
用水湿润
然后稍稍用力即可把玻璃管插入胶皮管.试管中放入的物质名称是
过氧化氢和二氧化锰
过氧化氢和二氧化锰
,写出该反应的化学方程式
⑥如要制取CO
2气体,应选择发生装置是
B
B
,收集装置是
E
E
.





 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案