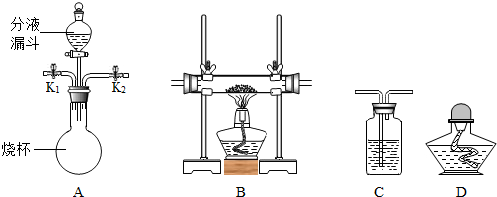
��2013?������һģ������������������Ӧ�ù㷺��
��1���������Ƴ��������������ý������������õ�
��չ
��չ
�ԣ�
��2������Ʒ�����������
�볱ʪ�Ŀ����Ӵ�
�볱ʪ�Ŀ����Ӵ�
����ϡ��������ⷴӦ�Ļ�ѧ����ʽ��
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
��
��3���ҹ����������������ʪ��ұ����ȡͭ�Ĺ��ң���������ͭ��Һ��Ӧ�Ļ�ѧ����ʽ��
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
����ҵ��ұ�������ǽ�����ʯ����Ҫ�ɷ���Al
2O
3��������������ͨ��ֽ⣬�䷴Ӧ�Ļ�ѧ����ʽ��
��
��4���������ֽ���������ɵĻ�����100gijϡ�����м���û�������������������������������ϵ��ͼ��ʾ��
����˵����ȷ����
acd
acd
������ţ���
a���������ΪZn��Al����m������0.2g
b���������ΪZn��Cu����mһ������0.2g
c���������ΪFe��Al����ϡ������������������һ������7.3%
d���������ΪFe��Cu��mΪ0.1g����û������Fe����������һ����50%

 ��2013?������һģ������������������Ӧ�ù㷺��
��2013?������һģ������������������Ӧ�ù㷺��


 ��2013?������һģ��ʳ���������������о��й㷺����;��
��2013?������һģ��ʳ���������������о��й㷺����;��