
| ||
| ||
| ||
| ||
| 100 |
| 44 |
| x |
| 4.4g |
| 12.5g-10g |
| 12.5g |


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:
请依据下列信息回答有关问题:
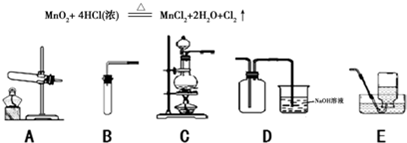
Cl2是一种黄绿色、具有刺激性气味、有毒的气体,其密度比空气的密度大。能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水。Cl2可用于漂白纸张、布匹以及消毒饮用水等。在实验室里常用下述反应制取氯气:

⑴写出氯气与氢氧化钠溶液反应的化学方程式: ;生成物中氯元素的化合价分别为 。
⑵实验室选择气体发生装置应考虑的因素有哪些?
⑶如上图,在实验室里制取氯气应选择的发生装置是 (填字母);收集氯气选用D装置,请推测其中氢氧化钠溶液的作用是 。
⑷如上图,若选用B、E组合在实验室可制取 气体,反应方程式为 。
⑸12.5g大理石与稀盐酸完全反应后,可生成二氧化碳气体4.4g,请计算大理石中杂质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:2012届河南省中招考试说明解密预测(五)化学试卷(带解析) 题型:单选题
请依据下列信息回答有关问题:
Cl2是一种黄绿色、具有刺激性气味、有毒的气体,其密度比空气的密度大。能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水。Cl2可用于漂白纸张、布匹以及消毒饮用水等。在实验室里常用下述反应制取氯气: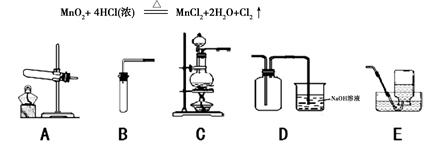
⑴写出氯气与氢氧化钠溶液反应的化学方程式: ;生成物中氯元素的化合价分别为 。
⑵实验室选择气体发生装置应考虑的因素有哪些?
⑶如上图,在实验室里制取氯气应选择的发生装置是 (填字母);收集氯气选用D装置,请推测其中氢氧化钠溶液的作用是 。
⑷如上图,若选用B、E组合在实验室可制取 气体,反应方程式为 。
⑸12.5g大理石与稀盐酸完全反应后,可生成二氧化碳气体4.4g,请计算大理石中杂质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
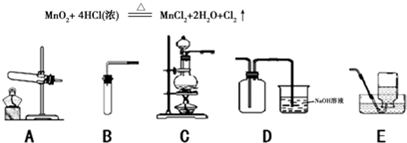
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com