
| 106 |
| x |
| 100 |
| 4g |
| 100 |
| 4g |
| 80 |
| y |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
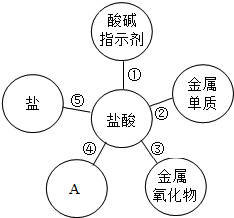 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
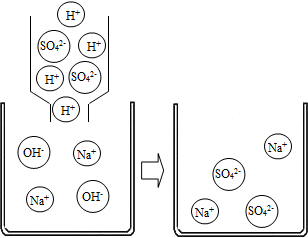 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).| 实验方案 | ①测溶液pH | ②滴加Na2CO3溶液 | ③滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,与标准比色卡比照,得pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

查看答案和解析>>
科目:初中化学 来源: 题型:
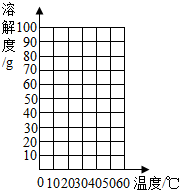 请根据你学习的有关溶液的知识,回答下列问题:
请根据你学习的有关溶液的知识,回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | A物质 | 30 | 35 | 45 | 50 |
| B物质 | 25 | 35 | 55 | 90 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
A、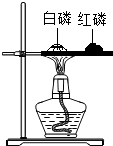 比较红磷、白磷着火点 |
B、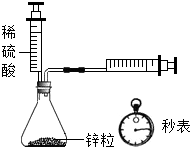 定量测定化学反应速率 |
C、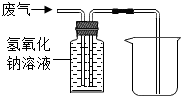 除去废气中的CO2,并收集CO |
D、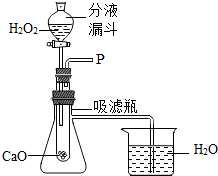 验证CaO和水反应的热效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com