
【题目】自来水生产中可以杀菌消毒的物质是
A、CO B、Cl2 C、明矾 D、活性炭
科目:初中化学 来源: 题型:
【题目】下列各组物质的溶液混合后,不能发生化学反应的是 ( )
A. Na2CO3和BaCl2 B. KOH和CuCl2
C. MgCl2和H2SO4 D. AgNO3和NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如图:
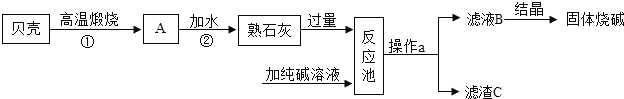
请回答下列问题:
(1)A的化学式是 ______.①的反应类型为: ______.
(2)写出步骤②发生反应的化学方程式②______.
(3)操作a的名称是______,结晶得到的固体烧碱中可能含有少量的______(写化学式).
(4)在工业上,熟石灰可用于生产烧碱.在农业上,它的一种用途是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示某些物质间的转化关系(反应条件均略去)。其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属。B、D、X、E均为无色气体。请回答:

(1)X是_______ (填化学式)。
(2)B物质固态时的名称是______,该物质在实际生活中的一种用途是____________。
(3)写出下列反应的化学方程式。
①F+X→B+G:________________________________________。
②C→D+E:__________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】观察颜色是化学实验关注的重点。下列物质与水充分混合后形成无色溶液的一组是
A. Ba(OH)2、CuCl2、NaCl B. HNO3、Fe2(SO4)3、BaCl2
C. NaNO3、HC1、Al2(SO4)3 D. KMnO4、Na2CO3、 Na2SO4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NaCl、KNO3两种固体物质的溶解度曲线如图所示。下列说法正确的是

A. 20℃时,NaCl的溶解度为31.6 g
B. 将10℃时两物质饱和溶液升温至30℃,溶液中溶质的质量分数都增大
C. 为了除去NaCl固体中混有的少量KNO3,可加热将其完全溶解后,再通过降温结晶、过滤来除之
D. 50℃时,将50g KNO3加入50g水中,充分溶解后溶液的质量为92.75g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一次化学实验中,两组同学都完成了硫酸铜溶液与氢氧化钠溶液反应的实验,但观察到了不同的实验现象。
【实验一】
实验组 | 甲组 | 乙组 |
实验操作 |
|
|
实验现象 | 产生蓝色沉淀 | 产生蓝绿色沉淀 |
⑴已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式______。
【提出问题】乙组产生的蓝绿色沉淀的成分是什么呢?
【查阅资料】
Ⅰ.碱式硫酸铜是绿色晶体,在水中溶解度极小,能溶于稀酸溶液。
Ⅱ.碱式硫酸铜的组成不固定,一般可用Cu2(OH)2SO4表示。
【猜想与假设】蓝绿色沉淀是碱式硫酸铜。
【实验二】
实验步骤 | 主要实验操作 | 现象及结论 |
① | 取乙组实验后的混合物过滤 | 得到蓝绿色沉淀 |
② | 取蓝绿色沉淀,用蒸馏水洗涤多次 | 无明显现象 |
③ | 向最后一次洗涤液中滴加BaCl2溶液 | 无沉淀产生 |
④ | 取洗涤后的蓝绿色沉淀于试管中,滴加稀盐酸 | 沉淀全部溶解,得到蓝绿色溶液 |
⑤ | 取少量蓝绿色溶液于试管中,滴加试剂X | 产生白色沉淀 |
实验结论:蓝绿色沉淀是碱式硫酸铜 | ||
【解释与结论】
⑵步骤③的实验目的是______。
⑶步骤④中的稀盐酸______(选填“能”或“不能”)用稀硫酸代替。
⑷步骤⑤中滴加的试剂X是______。
【反思与评价】
⑸甲组同学在本组实验的基础上进一步成下列实验:
①过滤,取蓝色沉淀于试管中;
②滴加______,沉淀颜色变为蓝绿色;
③重复实验二中的步骤①~⑤。
经实验验证,氢氧化铜也可以转化为碱式硫酸铜。此反应的化学方程式为______。
⑹乙组同学认为在自己组原有实验的基础上,继续滴加______,可以将碱式硫酸铜转变为氢氧化铜。通过实验,也验证了他们的猜想。
⑺为了确保氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜,实验的关键是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学科学常需要借助化学专用语言来描述,下列化学用语与其含义相符的是
A. 3N ----3个氮元素 B. O2 ----氧气 C. Al+3 ----铝离子 D. P----1个氟原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1774年,瑞典化学家舍勒在研究软锰矿(主要成分是二氧化锰)的过程中,将它与浓盐酸混合加热,制得了氯气(Cl2),同时生成二氯化锰和水。
(1)写出上述生成氯气的化学反应方程式_____________________________。
(2)研究小组的同学对氯水(氯气的水溶液)进行了探究。
①验证氯水的酸性:取少量氯水,向其中滴加___________(填一种酸碱指示剂),一开始可观察到滴加的指示剂在氯水中变____色。
②氯水具有漂白性,氯水中含有Cl2、HCl、HClO(次氯酸)。请你参与“氯水使品红试纸褪色”的研究。
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色。 猜想2:氯水中的Cl2使品红试纸褪色。
猜想3:氯水中的HCl使品红试纸褪色。 猜想4:氯水中的HClO使品红试纸褪色。
【实验探究】
实验操作 | 实验现象 | 结论 |
①用水润湿品红试纸,观察 | 试纸不褪色 | 猜想1不成立 |
②把品红试纸放入__________的氯气中,观察 | 试纸不褪色 | 猜想2不成立 |
③把品红试纸放入 _______________中,观察 | 试纸不褪色 | 猜想3不成立 |
【结论】通过探究,同学们找到了氯水使品红试纸褪色的原因。
【思考】根据氯水具有漂白性可推测,实验①向氯水中滴加几滴指示剂后,最终观察到的现象是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com