
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
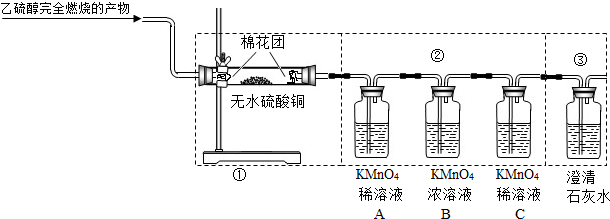
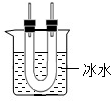 的连接顺序改为②、①、③,则不能检出的物质是
的连接顺序改为②、①、③,则不能检出的物质是
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
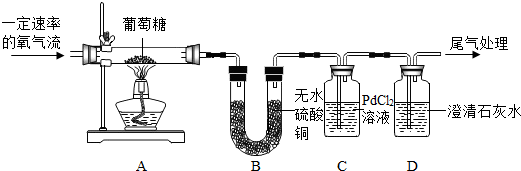
| 现象 | 结论或化学方程式 |
| 装置B中的无水硫酸铜变蓝色 | 它燃烧生成了 水 水 |
PdCl2溶液中出现了黑色的金属 PdCl2溶液中出现了黑色的金属 |
它燃烧生成了CO |
| 装置D中的澄清石灰水变浑浊 | 它燃烧生成了CO2,装置D中发生反应的化学方程式为: CO2+Ca(OH)2═CaCO3↓+H2O CO2+Ca(OH)2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2011-2012学年河南省洛阳市第二实验中学九年级第二学期月考化学试卷 题型:填空题
学习化学,使我变得聪明,我知道了:实验室用高锰酸钾制氧气结束时为了防止水倒吸使试管炸裂,应当 ;做一氧化碳还原氧化铁的实验开始时先 再加热。煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露。乙硫醇在煤气燃烧过程中也可充分燃烧,其反应方程式为2C2H5SH + 9O2点燃 4CO2 + 2X + 6H20,根据化学方程式,可判断出X的化学式为 。
查看答案和解析>>
科目:初中化学 来源:2009年全国中考真题分类汇编专题一信息给予题 题型:填空题
大龙在公园看到绿化工人往树干上涂抹具有杀菌杀虫作用的悬浊液,对其成份产生了好奇,于是他带回了一些样本进行研究。
信息提示:许多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这叫做焰色反应。如:钠——黄色;钙——砖红色;钾——紫色;钡——黄绿色
Ⅰ猜想与假设:该制剂可能为波尔多液
Ⅱ实验探究:
|
序号 |
实验步骤 |
实验现象 |
|
① |
取样,将其置于大试管中,加入一定量水,静置片刻 |
上层有黄色固体漂浮,中层为无色液体,下层有较多白色固体 |
|
② |
取少量中层液体滴加无色酚酞试液 |
无色酚酞试液变红 |
|
③ |
另取少量中层液体进行焰色反应 |
火焰呈现砖红色 |
|
④ |
取少量黄色固体灼烧 |
燃烧,放热,产生淡蓝色火焰,有刺激性气味 |
|
⑤ |
向下层白色固体中滴加足量稀盐酸 |
固体完全溶解,但仅产生少量气泡 |
Ⅲ实验结论:
(1)根据上述实验①,可以判断该悬浊液中 ▲ (填“含”或“不含”)硫酸铜;
(2)根据上述实验 ▲ (填序号),可以判断该悬浊液中含有氢氧化钙;
(3)根据上述实验④,可以判断黄色固体是 ▲ ;
(4)写出⑤中发生的所有反应的化学方程式: ▲ 。
答案:(1)不含 (2)②③ (3)硫(或硫磺)(各1分)
(4)Ca(OH)2+2HCl=CaCl2+2H2O CaCO3+2HCl=CaCl2+H2O+C02↑(各2分)
4.(2009常州市)小黄用右图装置测定铜锌合金中锌的质量分数和锌的相对原子质量。主要实验步骤如下(必要的固定装置已略去):
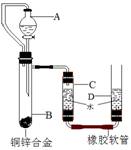
①连接装置并检查装置气密性;
②加入药品和水;
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加试剂至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥将B中剩余固体过滤、洗涤、干燥并称重,称得剩余固体质量为W g。
(1)A仪器的名称为 ▲ ;
(2)B中发生的反应的化学方程式为: ▲ ;
(3)小黄在实验前将块状的铜锌合金磨成粉末状,其目的是: ▲ ;
(4)如何检验该装置的气密性: ▲ ;
(5)为使测得的气体体积更精确,记录C中液面刻度时,除使视线与凹液面的最低处相平外,还应 ▲ ;
(6)小黄发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是: ▲ ;
(7)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验: ▲ ;理由是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com