


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源:不详 题型:填空题
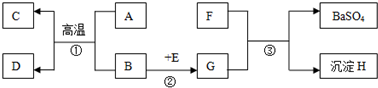
查看答案和解析>>
科目:初中化学 来源:不详 题型:多选题
| A.Cl-一定存在 |
| B.100mL溶液中K+的质量不小于2.34g |
| C.K+一定存在 |
| D.Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.Na+、Fe2+、NO3-、SCN- | B.Ca2+、K+、Cl-、NO3- |
| C.Al3+、K+、OH-、NO3- | D.Na+、Ca2+、SiO32-、Cl- |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.K2SO4、NaOH、NaCl | B.CuSO4、MgCl2、NaCl |
| C.NaOH、HCl、K2SO4 | D.Na2CO3、K2SO4、HCl |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.①④ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| H2SO4 |
| Zn |
| H2SO4 |
| CuO |
| A.消耗等质量的Zn、H2SO4、CuO |
| B.消耗的只有CuO质量相同 |
| C.过程中产生的ZnSO4质量相同 |
| D.所有反应类型都相同 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 物质 | 凝固点 | 沸点 |
| 水银 | -39℃ | 357℃ |
| 酒精 | -117℃ | 78℃ |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com