��2012?������ij��ѧ��ȤС���ͬѧ������������ֽ���������ȡ������ʵ���װ�ã�

�ش��������⣺
��1��ʵ�����ø��������ȡ����ʱ��Ӧѡ�õķ���װ����
A
A
����Ӧ�Ļ�ѧ����ʽ��
����ѡ��Cװ���ռ������������ռ�������Ӧ��
�������Ƴ�ˮ��
�������Ƴ�ˮ��
��Ȼ����
Ϩ��ƾ���
Ϩ��ƾ���
��
��2��ʵ���ҳ���ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼���䷴Ӧ�Ļ�ѧ����ʽ��
CaCO3+2HCl�TCaCl2+CO2��+H2O
CaCO3+2HCl�TCaCl2+CO2��+H2O
��ѡ�õ��ռ�װ����
B
B
�������Ƿ������ķ�����
��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ȼ�ŵ�ľ��Ϩ��֤��������̼���ռ���
��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ���ȼ�ŵ�ľ��Ϩ��֤��������̼���ռ���
����Ҫ�õ�����Ķ�����̼���壬��Ҫ�õ�Fװ�ã���װ��Ӧװ����Լ���
Ũ����
Ũ����
��




 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д�

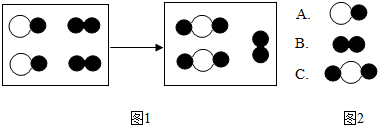
 ������ͼʾ�ش�
������ͼʾ�ش� ��
�� �ֱ��ʾ���ֲ�ͬԪ�ص�ԭ�ӣ��ش��������⣺
�ֱ��ʾ���ֲ�ͬԪ�ص�ԭ�ӣ��ش��������⣺