
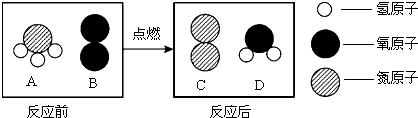
分析 利用反应前后分子变化的微观示意图可知,该反应的反应物A的分子由1个N原子和3个H原子构成的NH3分子,反应物B的分子由2个氧原子构成的O2分子;生成物C的分子由2个N原子构成的N2分子,生成物D的分子由1个O原子和2个H原子构成的H2O分子;则反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.据此分析解答即可.
解答 解:根据反应的微观图可该反应的反应物A的分子由1个N原子和3个H原子构成的NH3分子,反应物B的分子由2个O原子构成的O2分子;生成物C的分子由2个N原子构成的N2分子,生成物D的分子由1个O原子和2个H原子构成的H2O分子,写出反应物与生成物,然后配平使左右两边各原子的个数相等即可写出反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
(1)氧化物是含有两种元素,其中一种是氧元素的化合物,所以反应中H2O为氧化物;
(2)由分析知该反应的方程式是4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
故答案为:(1)D;(2)4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
点评 化合物为不同种元素组成的纯净物,化合物的分子则是由不同种原子构成的分子.分子构成与物质的分类关系:同种原子构成的分子为单质分子,不同种原子构成的分子为化合物分子.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:选择题
| A. | NaOH NaC1 CuSO4 HC1 | B. | KNO3 Na2SO4 NaOH KC1 | ||
| C. | KC1 Ba(NO3)2 HC1 CaC12 | D. | Na2CO3 Ba(OH)2 KNO3 Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 | B. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | ||
| C. | 氢气+氧气$\stackrel{点燃}{→}$水 | D. | 乙炔+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生产和使用剧毒农药 | B. | 用二氧化硫漂泊纸浆 | ||
| C. | 化工厂产生的废气向高空排放 | D. | 利用双氧水制氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
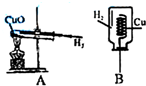 实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.
实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com