
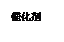 y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)
y = 0.8g 至少需要加入0.8g三聚氰胺 (1分)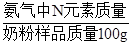 ×100%可完成计算;
×100%可完成计算; ×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;
×100%,计算100g奶粉中含蛋白质12g~25g时氮元素的质量分数范围;利用所取奶粉样品中N元素的质量分数与国家标准对比,判断所取奶粉是否合格;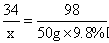
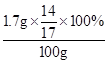 ×100%=1.4%
×100%=1.4%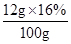 ×100%=1.92%
×100%=1.92%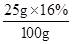 ×100%=4%
×100%=4%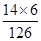 ×100%=(100g﹢y)×1.92%
×100%=(100g﹢y)×1.92% 

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.6.8g | B.5.6g | C.2.8g | D.1.2g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
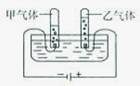
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com