
【题目】(6分)现有下列药品和实验仪器。
药品:石灰石、稀硫酸、稀盐酸
仪器如下:
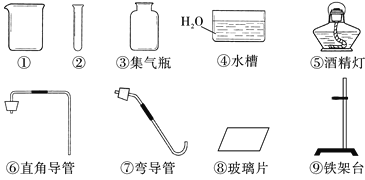
(1)写出未标注的仪器名称:① ,② 。
(2)实验室用题中药品制备并收集一瓶气体应选择的仪器是(填写仪器序号) ,反应的化学方程式为 。
【答案】[6分。(1)每空1分,(2)每空2分]
(1) ① 烧杯 ② 试管 (错别字不给分)
(2) ②③⑥⑧⑨ 或 ②③⑥⑧(不规定序号顺序)
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
【解析】
(1)根据仪器的名称和用途回答.
(2)根据给出的药品和各种气体制取的反应原理分析出所能制取的气体,再根据药品的状态和反应条件确定气体发生装置,根据气体的溶解性、密度等性质确定收集装置,根据反应原理涉及的反应物、生成物种类和反应条件写出化学方程式.
解答:解:(1)①是较大量试剂的反应容器,也可用来配溶液,叫烧杯,②是少量试剂的反应容器,叫试管.
(2)根据药品石灰石、稀硫酸、稀盐酸可知,能用来制二氧化碳,原理是碳酸钙和稀盐酸在常温下反应生成氯化钙、水和二氧化碳,方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;石灰石是固体,盐酸为液体,反应条件是常温,发生装置应由②⑨⑥组成,二氧化碳密度比空气大,能溶解于水且和水反应,所以用向上排空气法,收集装置由组成③⑧.
故答案为:(1)①烧杯;②试管;(2)②③⑥⑧⑨;CaCO3+2HCl=CaCl2+H2O+CO2↑


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】某化学小组用一定量 AgNO3 和 Cu(NO3)2 的混合溶液进行了如图实验,已知溶液甲呈蓝色。
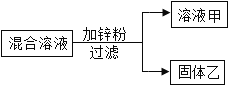
(1)向固体乙上滴加盐酸时_____(填“有”或“没有”)气泡产生。
(2)原混合溶液的质量比溶液甲的质量_____(填“大”“小”或“无法判断”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图实验判断下列说法错误的是( )
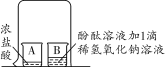
A. 浓盐酸有挥发性
B. 分子在不断运动
C. B烧杯溶液的颜色会改变
D. 实验后B烧杯内溶液颜色为无色,说明二者恰好完全反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)小华按右图配方自做一瓶清凉甘甜的汽水。
根据图中信息回答:

(1)小苏打中含有的金属元素的名称是 。
(2)打开汽水瓶盖产生气体的主要成分是 ,
该气体由柠檬酸与 反应生成。
(3)白糖的主要成分是C12H22O11,C12H22O11属于 ,(填“有机物”或“无机物”),其中 碳、氢、氧三种元素的质量比是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学发现一瓶没有塞上瓶塞的过氧化氢溶液,对该溶液中是否有过氧化氢的剩余,与同学们一起进行如下探究实验。
(猜想与假设)
猜想⑴:该溶液中有过氧化氢的剩余。猜想⑵:该溶液中没有过氧化氢的剩余。
(方案讨论)为了验证猜想,甲、乙、丙三同学分别提出如下方案
甲:取适量试剂于试管中,伸入带火星的木条,若带火星的木条复燃,则猜想(1)成立,若带火星的木条不复燃,猜想(2)成立.
同学们认为此方案不行,原因是____________________。
乙:取少量二氧化锰于试管中,加入与甲等量的试剂,若有气泡产生,则猜想(1)成立,若无气泡产生则猜想(2)成立,理由是______(写化学反应的文字表达式)
丙:
操作 | 现象 | 结论 |
取与甲等量试剂于试管中,加热,伸入带火星的木条 | __________________ | 猜想(1)成立 |
(反思与交流)1、敞口放置的试剂容易变质,所以要______保存。
2、二氧化锰在过氧化氢的分解过程中起________作用。除此之外能改变化学反应速率的方法还可以______________
查看答案和解析>>
科目:初中化学 来源: 题型:
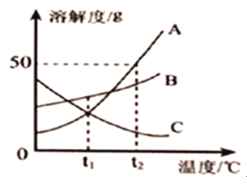
【题目】A、B、C三种固体物质的溶解度曲线如图所示。请回答下列问题。
(1)t1℃时,溶解度相同的物质是_____。
(2)若保持溶液质量不变,将C的饱和溶液变为不饱液的方法是_____。
(3)t2℃时,把50gA放入50g水中,所得溶液中溶质和溶液的质量比为_____(填最简整数比)。
(4)将t2℃时等质量的A、B、C三种物质的饱和溶液,降温度温至t1℃时所得溶液中溶剂质量由大到小顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】复印用的墨粉中含有Fe3O4粉末。制备Fe3O4的主要流程如下。
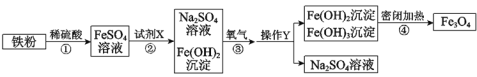
(1)①中发生反应的化学方程式为______。
(2)试剂X为______。
(3)操作Y为______。
(4)流程③反应前后,各物质中元素化合价发生改变的是______(填元素符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是用途广泛的化工原料,下图为硫酸工业的主要流程。

请回答下列问题:
(1)沸腾炉中,发生反应的方程式为:4FeS2 + ____ _____= 2Fe2O3 + 8SO2
(2)在接触室发生的反应中,化合价发生改变的元素有____________。
(3)吸收塔中常用98.3%的硫酸吸收SO3,主要反应为SO3 + H2O H2SO4,则所得产品中硫酸的浓度____________98.3%(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com