
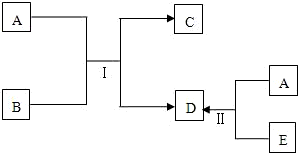
 化学美无处不在(如对称美,周期美、相似美),只要你学习方法巧妙(如对比、归纳、联想),你不仅感到化学学习其乐无穷,而且在精神上美不胜收.A、B、C、D、E为初中化学中常见的物质,其中A、C、E为单质,它们之间在一定条件下的转化关系如下图所示.
化学美无处不在(如对称美,周期美、相似美),只要你学习方法巧妙(如对比、归纳、联想),你不仅感到化学学习其乐无穷,而且在精神上美不胜收.A、B、C、D、E为初中化学中常见的物质,其中A、C、E为单质,它们之间在一定条件下的转化关系如下图所示. 2H2O.
2H2O. 2Cu+CO2↑(其他金属氧化物也可以).
2Cu+CO2↑(其他金属氧化物也可以). 2H2O.
2H2O. 2Cu+CO2↑(其他金属氧化物也可以).
2Cu+CO2↑(其他金属氧化物也可以).

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:初中化学 来源: 题型:
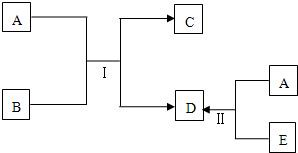 化学美无处不在(如对称美,周期美、相似美),只要你学习方法巧妙(如对比、归纳、联想),你不仅感到化学学习其乐无穷,而且在精神上美不胜收.A、B、C、D、E为初中化学中常见的物质,其中A、C、E为单质,它们之间在一定条件下的转化关系如下图所示.
化学美无处不在(如对称美,周期美、相似美),只要你学习方法巧妙(如对比、归纳、联想),你不仅感到化学学习其乐无穷,而且在精神上美不胜收.A、B、C、D、E为初中化学中常见的物质,其中A、C、E为单质,它们之间在一定条件下的转化关系如下图所示.查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
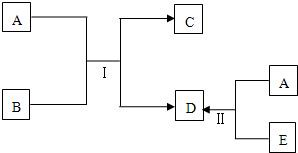
查看答案和解析>>
科目:初中化学 来源:2007年福建省厦门市思明区中考化学模拟试卷(解析版) 题型:填空题
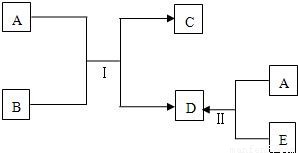
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com