
| 40 |
| x |
| 36.5 |
| 36.5g |
| 58.5 |
| y |
| 36g |
| 100g |
| 58.5g-z |
| 100g+100g-58.5g |
| 36g |
| 100g+36g |


科目:初中化学 来源: 题型:阅读理解
 请根据下面有关信息,按题目要求回答问题:
请根据下面有关信息,按题目要求回答问题:
| ||
. |
| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 请根据下面有关信息,按题目要求回答问题:
请根据下面有关信息,按题目要求回答问题: NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:
NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
查看答案和解析>>
科目:初中化学 来源:2012年江苏省苏州市相城区中考化学模拟试卷(解析版) 题型:填空题
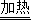 NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:
NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:| 时间/s | 20 | 30 | 40 | 60 | 80 | 100 | 120 | |
| 增加的质量/g | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
请根据下面有关信息,按题目要求回答问题:
(1)将放浓硫酸的试剂瓶露置在空气中一段时间后溶液的质量分数会 (填变大或变小)
(2)某厂以流量10L.s-1排出含硫酸9.8%的工业废水,现往该废水中排入含氢氧化钠2%的工业废水将其酸性中和后再排出。要使处理后的废水pH约为7,则氢氧化钠的流量应当为 (假设含酸废水的密度和含碱废水的密度约为1g.cm-3)
(3)四种氮肥:(NH4)2SO4、NH4HCO3、NH4NO3、CO(NH2)2(尿素),含氮量最低是 (填名称)
(4)为检验糖尿病患者的尿液,医院要配置8%的CuSO4溶液。现有1![]() 6g硫酸铜同体,可配置该硫酸铜溶液 g,需水
6g硫酸铜同体,可配置该硫酸铜溶液 g,需水 ![]() ml(水的密度为1.0g.cm-3)。
ml(水的密度为1.0g.cm-3)。
(5)火力发电厂用石灰浆吸收废气中的二氧化硫,以防止污染环境,其发生发应的化学方程式为2CaCO3+2SO2+O2=2CaSO4+2CO2.若100克废气中含有1.6克二氧化硫,则处理1000克这种废气需要含碳酸钙80%的石灰石 克.
(6)某校化学兴趣小组为测定某硝酸铵样品的纯度,将样品溶于水后,再加入氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH![]() NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:
NaNO3+H2O+NH3↑)。把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质最,结果如下表所示:
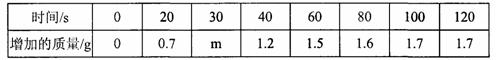
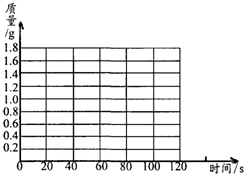
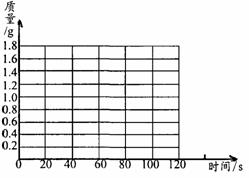
(a)请在下面的坐标纸上,以反应时间为横坐标, 以产生的NH3质量为纵坐标,画山能够表明产生气体的质量随时间变化的关系曲线:
(b)表中m约为 ;
 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com