
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:初中化学 来源: 题型:
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.查看答案和解析>>
科目:初中化学 来源:2013届江苏省南京市高淳县九年级第一学期期末调研检测化学试卷(带解析) 题型:填空题
(10分)铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀,原因是 。
(2)现有这三种金属,用下列试剂验证金属活动性顺序,能达到目的是 (填
序号)。
A.氯化铜溶液 B.氯化亚铁溶液 C.氯化铝溶液
(3)金属与酸反应的剧烈程度与许多因素有关。下图是20℃时相同质量的铁粉、铁片、
铝粉、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。
①写出铝与15%的盐酸反应的化学方程式 。
②根据上图推测,金属A是 (填字母序号)。
a.铝片 b.铝粉 c. 铁片 d.铁粉
③金属B与10%的稀盐酸反应的现象是:产生气泡、固体量减少、 。
④图中铝片、铁片分别与15%的稀盐酸完全反应,产生的氢气质量之比为 。
由此可以分析、归纳出影响金属与酸反应速率的因素有:金属的种类、 和酸的浓度。
(4)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(精确到小数点后1位)计算过程 。
查看答案和解析>>
科目:初中化学 来源:2012-2013学年江苏省南京市高淳县九年级第一学期期末调研检测化学试卷(解析版) 题型:填空题
(10分)铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀,原因是 。
(2)现有这三种金属,用下列试剂验证金属活动性顺序,能达到目的是 (填
序号)。
A.氯化铜溶液 B.氯化亚铁溶液 C.氯化铝溶液
(3)金属与酸反应的剧烈程度与许多因素有关。下图是20℃时相同质量的铁粉、铁片、
铝粉、铝片分别与足量稀盐酸完全反应,产生氢气的质量与时间的关系图。
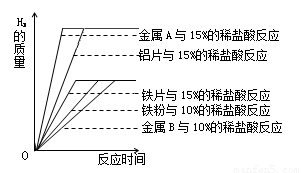
①写出铝与15%的盐酸反应的化学方程式 。
②根据上图推测,金属A是 (填字母序号)。
a.铝片 b.铝粉 c. 铁片 d.铁粉
③金属B与10%的稀盐酸反应的现象是:产生气泡、固体量减少、 。
④图中铝片、铁片分别与15%的稀盐酸完全反应,产生的氢气质量之比为 。
由此可以分析、归纳出影响金属与酸反应速率的因素有:金属的种类、 和酸的浓度。
(4)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(精确到小数点后1位)计算过程 。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com